肾上腺素能依赖性尖端扭转性室性心动过速
病因
(一)发病原因
既往将ADTdp分为下列三种类型:
1.Jervell-Lange-Nielson综合征(JLNS) 特点是伴有先天性耳聋,Q-T间期延长,T波异常,在紧张和应激状态下出现尖端扭转性室性心动过速(TDP)或心室颤动,甚至晕厥,猝死,系常染色体隐性遗传性疾病。
2.Romano-Ward综合征(RWS) 为常染色体显性遗传性疾病,不伴有耳聋,余与JLNS相同,Ganstorp综合征为RWS的亚型,表现为无先天性耳聋,伴血清钾降低。
3.散发型 无家族史,听力正常,其余同JLNS。
(二)发病机制
近年来认识到基因突变是其遗传基础的基本动因,ADTdp具有遗传异质性,目前已知至少有6种LQTS(LQT1~LQT6)的变异位点为常染色体显性遗传,其中5种已在染色体上定位,4种已确立相关的突变基因,JLNS属于LQT1,相关突变基因为KVLQT1,当JLNS患者的父母双亲都含有KVLQT1,并从双亲遗传获得异常基因为纯合子时,KVLQT1使心脏离子通道功能异常即钾通道调控功能异常,使心肌复极明显延迟表现为Q-T间期明显延长,属常染色体显性遗传,其基因携带者也只有在低钾等条件时才发生TDP,KVLQT1还通过编码听力元件而出现先天性听力异常及耳聋,而耳聋属常染色体隐性遗传,由于形成JLNS的条件如此特殊,所以JLNS很少见,其他各型LQT即构成RWS,所以RWS是由多种遗传缺陷所致,属常染色体显性遗传,其已知的相关基因有LQT2,LQT3(HERG),LQT4(SCN5A),LQT5,LQT6(KCNE4)。
 缺陷基因介导细胞膜离子通道调控功能异常:SCN5A编码钠通道使Na 内向电流增加,其离子介导有可能与Cl-异常有关,KVLQT1,KCNE1及HERG编码钾通道,使K 外向电流降低,因此无论哪一种或多种基因突变均可导致K 外流减少,和(或)Na 内流增加即内向电流增大,致使动作电位2相及3相时程延长及膜电位增高,产生复极延迟及不完全,心电图表现为Q-T间期延长,TU波异常,由于这种电异常产生后除极(特别是早期后除极EAD)易达阈电位而引起触发性心律失常,表现为TDP或心室颤动,EAD与TDP的形成和维持与心肌中层M细胞也有关,心律失常的维持与折返机制有关。
缺陷基因介导细胞膜离子通道调控功能异常:SCN5A编码钠通道使Na 内向电流增加,其离子介导有可能与Cl-异常有关,KVLQT1,KCNE1及HERG编码钾通道,使K 外向电流降低,因此无论哪一种或多种基因突变均可导致K 外流减少,和(或)Na 内流增加即内向电流增大,致使动作电位2相及3相时程延长及膜电位增高,产生复极延迟及不完全,心电图表现为Q-T间期延长,TU波异常,由于这种电异常产生后除极(特别是早期后除极EAD)易达阈电位而引起触发性心律失常,表现为TDP或心室颤动,EAD与TDP的形成和维持与心肌中层M细胞也有关,心律失常的维持与折返机制有关。
JLNS多在情绪激动,精神紧张,运动及劳累导致心率增快时出现TDP,表现为发作性晕厥甚至猝死,此与交感神经张力增高,儿茶酚胺增多促使钙通道开放,Ca2 内流增多有关,因其促使内向电流增大,加重了细胞膜内外离子流的失衡,更易于产生后除极特别是EAD及触发性心律失常,有的ADTdp平时不表现出Q-T间期延长,只有当交感神经张力增高,内向电流增大更为明显时才出现,因此,将JLNS与RWS及与其并发的TDP称之为肾上腺素依赖性TDP,但也有少数ADTdp患者是在睡眠或安静状态发病(为HERG及SCN5A基因缺陷类型),属于间歇依赖性;同时肾上腺素能神经兴奋亦能促使药物所致继发性LQTS患者TDP的发作,说明在发生机制上两型均有少许交叉。
症状
ADTdp少见,美国每年约有3000例儿童及青少年死于本病,约2/3基因携带者发生晕厥,猝死率约为15%,发病年龄从出生后数天至50岁,TDP的首发病年龄阶段多在婴儿及儿童期,主要表现为发作性晕厥及猝死,晕厥几乎都是发生在交感神经高度紧张或张力突然变化的情况下(发作呈肾上腺素能依赖性特点),例如剧烈运动,劳累,排便,精神紧张,疼痛,恐惧,焦虑,噩梦,声光刺激等,心率逐渐加快并出现室性期前收缩,从而诱发TDP,有时可转化为心室颤动而猝死,症状轻者意识不丧失,仅出现黑矇,眩晕,可有视力模糊,忧虑,呻吟,喊叫等,重者发生晕厥,意识丧失,抽搐,尿失禁,猝死,易被误诊为癫痫,发作后24h内常有倦怠或嗜睡,TDP或晕厥发作次数多至一天数次,少则数年1次或终生仅发作1~2次,随年龄增长,Q-T间期逐渐缩短,发作次数相应减少,JLNS伴有先天性耳聋及骨骼畸形,家族成员中可见有Q-T间期延长,不明原因晕厥发作或猝死者,临床上可将肾上腺素能依赖性TDP分为下列3型:
1.典型性
本病初为婴儿和儿童期,也可见延迟至30岁或成年期,主要特征是发作性晕厥,其原因是TDP引起,常因突然运动,恐惧,疼痛,惊吓或情绪激动诱发,呈肾上腺素能依赖性,易误认为癫痫。
2.不典型性
此型发生率比典型性高,在运动和精神紧张时U波增大并出现TDP,临床表现轻型多,常因运动试验或因室性期前收缩接受ⅠA类抗心律失常药治疗发生TDP,激发试验如运动试验和滴注异丙肾上腺素可诱发。
3.中间型
LQTS 部分患者在肾上腺素能兴奋时发生TDP,在出现心跳长间歇时也发生TDP,前者治疗用β受体阻滞药,后者治疗可用异丙肾上腺素终止TDP,另一部分人心电图有明显U波,TDP发作时没有长间歇,与体力负荷或情绪激动亦无明显关系。
检查
1.心电图检查特点
A. Q-T间期延长:传统诊断标准为Q-T间期及QTc≥0.44s,1993年提出的国际通用诊断标准为男性≥0.45s,女性≥0.46s,为延长,本病患者Q-T间期延长通常是长期存在的,但其程度经常变化,有时可不延长,随着年龄的增大可渐有缩短,运动可使Q-T间期延长,Q-T间期的长短与突变基因的种类有关,LQTS1,LQTS2者Q-T间期多为正常,LQTS3,LQTS4者Q-T间期多为延长,在TDP发作前数秒至数分钟内,可见Q-T间期(QTc间期)明显延长,TU波明显异常,并可逐搏表现不同,逐天改变,甚至瞬息改变,TDP发作时Q-T间期大多>0.44s,少部分患者>0.60s。
B.T,U波形态异常:T波宽大,U波波幅增加,不同类型突变基因的LQTS亚型间T波形态可有不同,可表现为增宽,变尖及降低等,可出现T波电交替(即T波正向及负向交替出现),常出现在肾上腺素能依赖性TDT发作前,而间歇依赖型TDP无此特点,可作鉴别,它亦是识别高危患者的一个重要而客观的指标,U波亦可显著增高(>0.15mV为显著U波),亦可呈U波电交替,尤以出现QT(U)电交替更具诊断价值,TU振幅,QT电交替,可呈波动性改变,且与患者的疾病发展程度,剧烈运动及情绪激动有密切关系,复杂的TU形态变化常是严重心律失常出现的前兆。
②在发作间歇期内或Q-T间期正常时:用促使交感神经张力增加的方法,如运动试验,冷加压试验或瓦氏动作,或静脉滴注异丙肾上腺素等增加心率的措施时,可使原有的Q-T间期延长者更延长,Q-T间期正常者发生延迟,T波增大,增宽,U波振幅增加,并可诱发TDP,Kadise(1990)提出,静息时QT正常而运动时异常延长是“潜在性LQTS”的概念,说明通过对LQTS患者家族运动试验,观察T,U波的变化,对其是否发病具有一定的预测作用。
③发作间歇期内可见室性期前收缩或R-on-T室性期前收缩:基础心律多为窦性心律。
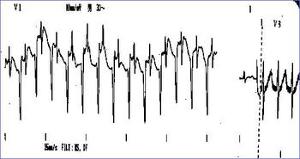 ④Q-T间期离散度大:常规导联中最长与最短Q-T间期之差值为Q-T间期离散度,反映心室复极的离散度(QTd),正常人均为89ms,LQTS患者人均为155ms。
④Q-T间期离散度大:常规导联中最长与最短Q-T间期之差值为Q-T间期离散度,反映心室复极的离散度(QTd),正常人均为89ms,LQTS患者人均为155ms。
(2)肾上腺素能依赖性TDP发作期心电图特点:发作时频率为150~180次/min,TDP可由R-on-T型(R-on-U型)室性期前收缩诱发,也可见于心室复极时间极度延长Q-T/R-R≥1时,匀齐而正常的心搏亦可落入心室异常延缓的复极期内诱发产生ADP,本型ADP没有一长一短周期的特点,这是与间歇依赖型ADP鉴别的主要依据之一。
诊断
1993年Schwarts提出计分法LQTS诊断标准,为目前国际上通用的诊断标准。
鉴别
尖端扭转型室性心动过速与其他多形性室速的鉴别甚困难,主要依据其QT间期延长,U波,常无严重的器质性心脏病,有特殊的病因,常反复发作并可自行终止等特点。
此外,须与一般室速或心室颤动相鉴别,一般室速表现为一系列形态几乎固定的宽大QRS波,ST段与T波可以辨认,发生往往不会自行停止;一般室速也可由RonT室早诱发,但室早配对间距较短,室颤时无法识别QRS波及ST段与T波,发作持续即死亡。
本病应与发作性晕厥和猝死的疾病鉴别,例如应与间歇依赖性TDP,预激综合征伴极速性心房颤动,特发性心室颤动,Brugada综合征,病态窦房结综合征及癫痫等相鉴别,应除外继发性Q-T间期延长。
并发症
治疗
(一)治疗
1.药物治疗
(1)β受体阻滞药:由于本型TDP的触发因素是交感神经性活动增高所致,肾上腺素能抑制剂可获最佳疗效。对于长期治疗或对急性发作治疗,β受体阻滞药是首选药物,常用能耐受的大剂量普萘洛尔(心得安)治疗,剂量为:1~2mg用5%葡萄糖液20ml稀释后缓慢静脉推注,若无效,再用0.5~0.75mg,每2分钟静脉推注1次,总量<5mg。注意普萘洛尔可致心衰加重、低血压、心动过缓、心脏停搏等,应在心电监护下密切观察。静注有效后口服,剂量从10mg,3次/d,逐渐增加到足量为3mg/kg。一般主张长期服用,减量时应逐渐减,不能突然停药。有报告在突然停药后可发生反跳,个别可发生猝死。大剂量普萘洛尔的耐受性个体差异较大,必须注意个体化。当耐受不了,而又未达到足量、TDP仍在发作的患者,可选用美托洛尔(Metoprolol或称美多心安,倍他乐克),先以5mg稀释(5%葡萄糖液20ml)后缓慢静脉推注,如无效,5min后可重复1次。或用萘羟心安(Nadolol)等。普萘洛尔用后可减少本型TDP的发作次数或完全控制发作,TU异常可恢复正常,QTc间期缩短。但有的Q-T间期仍延长。用普萘洛尔治疗后病死率由73%可降低至6%。在应用β受体阻滞药时,由于剂量较大,必须很好地监测,注意不良反应的出现,及时纠正。
(2)苯妥英钠:可用于经β受体阻滞药治疗无效的本型TDP。剂量为50~100mg,用注射用水稀释后缓慢静脉推注,每5~10分钟重复1次,直至心律失常消失或累积剂量达1000mg,改口服维持量,首日1000mg,第2、3天500mg,以后300~400mg/d。严重低血压、心力衰竭、心动过缓及高度房室传导阻滞者禁用。有主张苯妥英钠(35mg)与普萘洛尔(150mg),3次/d交替口服,也可控制发作,比单用一种药效果好。
(3)其他药物:少数病例对普萘洛尔(注射)无效,而用利多卡因或硫酸镁有效。维拉帕米、普罗帕酮仅个别有效。禁用儿茶酚胺类及延长复极的药物。
2.左侧颈交感神经切断术
对足量药物治疗无效者,可行左侧颈交感神经切断术。切除左侧星状神经节的下部及前3~5个胸节(保留星状神经节的上部,以避免发生Horner综合征),可使病死率降低7%。手术后仍应长期服用普萘洛尔。
3.植入心脏复律除颤器(ICD)
4.同步直流电击复律
当患者TDP持续发作,药物治疗无效或有可能发展为心室颤动、猝死者,应及时行电复律终止发作。
5.对缺陷基因分类进行治疗
对LQT1、LQT2型(即KXLQT、MINK及HERG缺陷基因)患者,应以钾通道为“靶点”进行治疗,如用Nicorandil(系钾通道开放剂)、补钾、补镁治疗。螺内酯也有效。对LQT3型(相关基因为SCNSA和部分HERG)患者,应以钠通道为“靶点”进行治疗,如美西律(Mexiletine)。治疗后,LQTS3组Q-T间期、QTc显著降低,而LQTS2组无效。对于LQTS2患者,因其与细胞外钾浓度升高激活HERG钾离子通道有关,此时补充钾盐可使复极异常得到纠正。
(二)预后
当QTc间期>0.60s、心动过速、有猝死病史、普萘洛尔治疗无效等指征为LQTS的高危指征,患者预后差,年死亡率为9%,首次发病即有30%~40%的患者死亡。未接受治疗的肾上腺素能依赖性TDP有症状患者的病死率可高达71%。治疗后可显著降低。
与未治疗者相比,β受体阻滞药长期治疗者显著减少晕厥发作和降低病死率,虽然其Q-T间期并不一致地缩短。经β受体阻滞药治疗的患者,以及做过左侧颈交感神经切断术的患者,总的晕厥发生率已下降到9%,猝死率已下降到1.5%。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。