柯萨奇病毒感染
概述
柯萨奇病毒是一种肠病毒,分为A和B两类,一般在夏秋季呈流行或散在发生,传播途径是经消化道、呼吸道,亦可通过血行经胎盘传播给胎儿。病毒开始在肠道、上呼吸道的内皮细胞和淋巴组织内复制,经血行传播,其亲嗜性靶器官为中枢神经系统,心脏、血管内皮细胞、肝、胰、肺、生殖器官、骨骼肌、皮肤黏膜等。
病因
(一)发病原因
柯萨奇病毒属于小核糖核酸病毒科的肠道病毒属,病毒颗粒为球形或卵圆形,直径为22~30nm,呈圆形颗粒状,病毒基因组为单股线状RNA,全长约6000~8500 bp,构成病毒核心,外壳呈20面体,立体对称,由32个壳粒组成,每个壳粒含有病毒核酸编码的四种壳蛋白VP1~VP4,在5ˊ端结合一个病毒基因蛋白Vpg,在Vpg之后接着一段长约740 bp的非编码区,柯萨奇病毒按照在乳鼠中病变的不同而分为A,B两组,A组原有24个血清型,其中第23型后来被划归艾柯病毒9型,尚存23个血清型,这些血清型皆可用中和试验和补体结合试验加以区别,A组病毒虽不具有共同的抗原,但有型间的交叉免疫性,如A3和A8,A11和A15,A13和A18之间可有交叉血清反应;相反,在6个B组病毒的血清型和A9之间,则有共同的群抗原,除少数毒株外,柯萨奇病毒不产生红细胞凝集素,因而不能采用血凝抑制试验来鉴定。
柯萨奇病毒对新生小白鼠有高度致病性,A组病毒引起骨骼肌广泛性肌炎和弛缓性瘫痪而于1周内死亡,B组病毒可引起灶性分布的肌炎,并可引起脂肪组织炎,脑炎,心肌炎,胰腺炎,肝炎和心内膜炎,乳鼠常出现全身震颤,痉挛和强直性瘫痪。
较年长的小白鼠可耐受B组病毒感染,但可通过使用肾上腺皮质激素而诱发胰腺炎,营养不良可使B3病毒在成年小白鼠中产生严重疾病,包括在心,脾,肝,脑中的持续性感染,淋巴组织萎缩,将有免疫力的小白鼠淋巴细胞转移至营养不良小白鼠体内,可保护该小白鼠抵抗B3病毒,防止严重后果的产生。
A7,A9和A16病毒亦可在猴肾细胞培养中生长,某些A组毒株可在人羊膜细胞,Hela细胞或RD细胞株中生长,但A1,A19和A22病毒则未能在任何细胞培养中繁殖,血液中短暂出现,并通过粪便排出持续2~5周之久,A14病毒在成年小白鼠和猴子中引起脊髓灰质炎样病变,A7病毒在猴子中则引起严重中枢神经系统病变和瘫痪。
在细胞培养中,B组病毒可引起细胞病变,受染细胞变圆,皱缩,胞核固缩,反光,最后退化而脱落,A组病毒不产生细胞病变。
(二)发病机制
病毒由肠道或呼吸道进入人体后在小肠,咽部的上皮细胞及附近淋巴组织内繁殖复制,达一定程度后侵入血循环中,形成第1次(次要)病毒血症,此时患者可出现轻度不适或全无症状,病毒随血流进入各种靶组织,并在其中继续繁殖,导致组织细胞发生损害;同时再次侵入血循环(第2次或主要病毒血症),使各种靶组织又一次遭到病毒的侵袭,临床症状一般发生于组织细胞损害出现后及第2次病毒血症时。
在潜伏期的后一阶段或前驱期,并在此后的1周左右,病毒可自咽洗液或咽拭中被分离出,自粪便或肛拭中分离出病毒的时期则较长,可达2周至1个月之久,少数病例甚至在病后70天仍呈阳性;患病后的第1周的阳性率最高,以后逐渐下降,病毒还可以从患者的脑脊液,疱浆液,血液,尿,胸腔积液,心包液,骨髓等处检出,在死亡者的各种脏器如心,脑,肝,脾,肾,睾丸,肌肉等中也可分离到病毒。
病毒在体内的不断繁殖复制使人体产生一种具有抑制病毒复制的干扰素,当干扰素及特异性中和抗体在血中出现时,病毒即自血循环中消失,唾液及肠分泌物中的分泌型IgA是各种免疫球蛋白中最早出现者,有阻抑病毒自消化道侵入体内的作用,继而在血中出现IgM,自病程第1周起迅速上升,而于3~4周内下降或消失,IgG型中和抗体于感染后7~14天出现,3~4周内达高峰,并可维持多年,补体结合抗体与中和抗体同时出现,但仅维持2~3个月。
部分柯萨奇病毒经呼吸道进入人体仅引起上呼吸道感染而无病毒血症,病毒局限于呼吸道黏膜表面,并随着呼吸道分泌物而排出,粪便中无病毒。
组织损伤主要通过病毒在细胞内复制产生抑制因子,抑制细胞核糖核酸和蛋白质合成,而导致细胞破坏,但在某些肠道病毒中,免疫应答引起的组织损伤可能是疾病迁延的原因,如在心肌炎时早期组织损伤可能由病毒复制引起,后期病变则与免疫应答有关。
柯萨奇和埃可病毒所引起的中枢神经系统病变与脊髓灰质炎病毒所引起的病变相似,但柯萨奇B组病毒则同时可引起灰质和白质的病变,在婴儿中,常累及脑干。
柯萨奇B组病毒引起的心肌炎表现为间质的单核细胞浸润,伴有一定程度的水肿和心肌纤维坏死,左心室扩张及肥厚,部分病例有心包炎,偶可引起心内膜炎,心包炎通常为纤维素性,但也有渗出性的,心内膜肉眼可见心瓣膜游离,边缘有疣状突出,镜下为致密纤维组织及慢性炎症细胞浸润。
表现
1.柯萨奇病毒A型感染
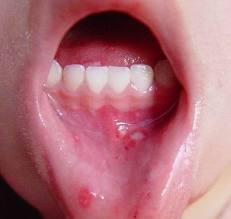 潜伏期1~3天,上呼吸道感染,起病急,流涕、咳嗽、咽痛、发烧,全身不适。典型症状为疱疹性咽峡炎,即在鼻咽部、会厌、舌和软腭部出现小疱疹,黏膜红肿,淋巴滤泡增生、渗出,扁桃体肿大,伴吞咽困难,食欲下降。皮疹可为疱疹和斑丘疹,主要分布于躯干外周侧、背部、四肢背面,呈离心性分布,尤以面部、手指、足趾、背部皮疹多见,故称手、足、口三联症。柯萨奇病毒A型感染儿童多见。临床表现除上述外,主要特点为急性发烧、皮疹。脑膜脑炎伴有Guillain-Barré综合征和急性病毒性心肌病。
潜伏期1~3天,上呼吸道感染,起病急,流涕、咳嗽、咽痛、发烧,全身不适。典型症状为疱疹性咽峡炎,即在鼻咽部、会厌、舌和软腭部出现小疱疹,黏膜红肿,淋巴滤泡增生、渗出,扁桃体肿大,伴吞咽困难,食欲下降。皮疹可为疱疹和斑丘疹,主要分布于躯干外周侧、背部、四肢背面,呈离心性分布,尤以面部、手指、足趾、背部皮疹多见,故称手、足、口三联症。柯萨奇病毒A型感染儿童多见。临床表现除上述外,主要特点为急性发烧、皮疹。脑膜脑炎伴有Guillain-Barré综合征和急性病毒性心肌病。
2.柯萨奇病毒B型感染
检查
并不是所有的血清型都适合的,只有属于以下情况之后的血清型才适合:
(2)已发现特征性临床表现如流行性胸痛,明显指示采用某些特定抗原(如B组病毒)来检测抗体时;或手、足、口腔病通常由柯萨奇A16型病毒所引起时。
(3)已分离出病毒,作为确定血清型时。
在所有的血清学检查方法中,中和试验是鉴定已分离病毒血清型最特异的方法。
2.外周血象
显示为白细胞总数正常或稍增多。
3.病毒分离法
诊断
 夏秋季流行,小儿居多,一家中多人发病等有参考意义,有近期内本地区流行的资料在诊断上尤有价值。
夏秋季流行,小儿居多,一家中多人发病等有参考意义,有近期内本地区流行的资料在诊断上尤有价值。
2.临床特征
一些有特征性的临床表现,如口腔内疱疹,胸痛或肌痛,心肌炎,脑膜炎,特殊皮疹等对协助诊断均有价值,白细胞总数正常,双峰热等也有一定参考意义。
当新生儿有任何流行性的严重疾病,以及新生儿突然发生心肺功能严重障碍时,均应考虑柯萨奇病毒感染的可能,在夏秋季遇原因不明的发热和(或)皮疹,特别当患者为婴幼儿时,也应怀疑柯萨奇病毒感染。
3.确诊依据
因健康人群的肠道内常有此类病毒,如仅在患者的粪便或肛拭中分离出柯萨奇病毒时,不能凭此而即下结论,宜以下列几点为确诊依据:
①从患者的各种体液或分泌物如脑脊液,血液,疱浆液,胸腔积液等,或尸检脏器如心,脑,肝,脾等中分离出病毒;
②用双份血清作中和试验(或其他血清学检查),抗体效价上升4倍以上;
③在患者中的病毒分离率远高于未接触患者的正常对照组;
④无其他已知病原体能引起此类综合征,而从患者的咽洗液,咽拭,粪便,肛拭等之中却能重复分离到同一病毒,并从周围接触者中也检出相同的病毒。
治疗
1、目前尚无特效的疫苗,因为其病毒血清型过多(有近70个型)。
2、主要是加强预防、隔离,尤其是夏季应加强病房空气消毒、积极治疗医护人员隐匿性感染;第一孕季感染的孕妇应作系统检查,排除胎儿畸形。
(1)远离传染源
重点是托幼机构和产房;特别注意怀柔的妇女,如果其患有肠道病毒性疾病,对新生儿有很大威胁。
(2)切断传播途径
养成良好的生活卫生习惯:自来水宜煮沸后饮用;避免在污水中游泳。
(3)保护易感者
主要是保户婴幼儿,可以尝试肌内注射丙种球蛋白3~6ml或者口服脊髓灰质炎疫苗OPV以防感染。
目前尚缺乏特效治疗,应强调一般及支持疗法。
(1)一般情况下,可试用利巴韦林或干扰素。
(2)新生儿心肌炎的进展迅速,应给氧及保持安静,出现心力衰竭时及早采用快速洋地黄疗法。
(3)有惊厥及严重肌痛者给予镇静剂或普鲁卡因局部封闭,麻醉剂如吗啡、哌替啶等不宜轻易采用。
(4)给予适当的抗菌药物以防止继发细菌感染。
(5)如果有心肌炎伴心力衰竭、心源性休克、严重心律失常(如高度房室传导阻滞、病态窦房结综合征等)、心包炎患者,则可以考虑肾上腺皮质激素。值得注意的是,鉴于此激素可抑制机体免疫功能,有利于病毒的复制,因此一般病例不宜采用。
预防
加强预防、隔离,尤其是夏季应加强病房空气消毒、积极治疗医护人员隐匿性感染。第一孕季感染的孕妇应作系统检查,排除胎儿畸形。目前尚无有效疫苗。
(一)发病原因
柯萨奇病毒属于小核糖核酸病毒科的肠道病毒属,病毒颗粒为球形或卵圆形,直径为22~30nm,呈圆形颗粒状,病毒基因组为单股线状RNA,全长约6000~8500 bp,构成病毒核心,外壳呈20面体,立体对称,由32个壳粒组成,每个壳粒含有病毒核酸编码的四种壳蛋白VP1~VP4,在5ˊ端结合一个病毒基因蛋白Vpg,在Vpg之后接着一段长约740 bp的非编码区,柯萨奇病毒按照在乳鼠中病变的不同而分为A,B两组,A组原有24个血清型,其中第23型后来被划归艾柯病毒9型,尚存23个血清型,这些血清型皆可用中和试验和补体结合试验加以区别,A组病毒虽不具有共同的抗原,但有型间的交叉免疫性,如A3和A8,A11和A15,A13和A18之间可有交叉血清反应;相反,在6个B组病毒的血清型和A9之间,则有共同的群抗原,除少数毒株外,柯萨奇病毒不产生红细胞凝集素,因而不能采用血凝抑制试验来鉴定。
柯萨奇病毒对新生小白鼠有高度致病性,A组病毒引起骨骼肌广泛性肌炎和弛缓性瘫痪而于1周内死亡,B组病毒可引起灶性分布的肌炎,并可引起脂肪组织炎,脑炎,心肌炎,胰腺炎,肝炎和心内膜炎,乳鼠常出现全身震颤,痉挛和强直性瘫痪。
较年长的小白鼠可耐受B组病毒感染,但可通过使用肾上腺皮质激素而诱发胰腺炎,营养不良可使B3病毒在成年小白鼠中产生严重疾病,包括在心,脾,肝,脑中的持续性感染,淋巴组织萎缩,将有免疫力的小白鼠淋巴细胞转移至营养不良小白鼠体内,可保护该小白鼠抵抗B3病毒,防止严重后果的产生。
A7,A9和A16病毒亦可在猴肾细胞培养中生长,某些A组毒株可在人羊膜细胞,Hela细胞或RD细胞株中生长,但A1,A19和A22病毒则未能在任何细胞培养中繁殖,血液中短暂出现,并通过粪便排出持续2~5周之久,A14病毒在成年小白鼠和猴子中引起脊髓灰质炎样病变,A7病毒在猴子中则引起严重中枢神经系统病变和瘫痪。
在细胞培养中,B组病毒可引起细胞病变,受染细胞变圆,皱缩,胞核固缩,反光,最后退化而脱落,A组病毒不产生细胞病变。
(二)发病机制
病毒由肠道或呼吸道进入人体后在小肠,咽部的上皮细胞及附近淋巴组织内繁殖复制,达一定程度后侵入血循环中,形成第1次(次要)病毒血症,此时患者可出现轻度不适或全无症状,病毒随血流进入各种靶组织,并在其中继续繁殖,导致组织细胞发生损害;同时再次侵入血循环(第2次或主要病毒血症),使各种靶组织又一次遭到病毒的侵袭,临床症状一般发生于组织细胞损害出现后及第2次病毒血症时。
在潜伏期的后一阶段或前驱期,并在此后的1周左右,病毒可自咽洗液或咽拭中被分离出,自粪便或肛拭中分离出病毒的时期则较长,可达2周至1个月之久,少数病例甚至在病后70天仍呈阳性;患病后的第1周的阳性率最高,以后逐渐下降,病毒还可以从患者的脑脊液,疱浆液,血液,尿,胸腔积液,心包液,骨髓等处检出,在死亡者的各种脏器如心,脑,肝,脾,肾,睾丸,肌肉等中也可分离到病毒。
病毒在体内的不断繁殖复制使人体产生一种具有抑制病毒复制的干扰素,当干扰素及特异性中和抗体在血中出现时,病毒即自血循环中消失,唾液及肠分泌物中的分泌型IgA是各种免疫球蛋白中最早出现者,有阻抑病毒自消化道侵入体内的作用,继而在血中出现IgM,自病程第1周起迅速上升,而于3~4周内下降或消失,IgG型中和抗体于感染后7~14天出现,3~4周内达高峰,并可维持多年,补体结合抗体与中和抗体同时出现,但仅维持2~3个月。
部分柯萨奇病毒经呼吸道进入人体仅引起上呼吸道感染而无病毒血症,病毒局限于呼吸道黏膜表面,并随着呼吸道分泌物而排出,粪便中无病毒。
组织损伤主要通过病毒在细胞内复制产生抑制因子,抑制细胞核糖核酸和蛋白质合成,而导致细胞破坏,但在某些肠道病毒中,免疫应答引起的组织损伤可能是疾病迁延的原因,如在心肌炎时早期组织损伤可能由病毒复制引起,后期病变则与免疫应答有关。
柯萨奇和埃可病毒所引起的中枢神经系统病变与脊髓灰质炎病毒所引起的病变相似,但柯萨奇B组病毒则同时可引起灰质和白质的病变,在婴儿中,常累及脑干。
柯萨奇B组病毒引起的心肌炎表现为间质的单核细胞浸润,伴有一定程度的水肿和心肌纤维坏死,左心室扩张及肥厚,部分病例有心包炎,偶可引起心内膜炎,心包炎通常为纤维素性,但也有渗出性的,心内膜肉眼可见心瓣膜游离,边缘有疣状突出,镜下为致密纤维组织及慢性炎症细胞浸润。
(一)发病原因
柯萨奇病毒属于小核糖核酸病毒科的肠道病毒属,病毒颗粒为球形或卵圆形,直径为22~30nm,呈圆形颗粒状,病毒基因组为单股线状RNA,全长约6000~8500 bp,构成病毒核心,外壳呈20面体,立体对称,由32个壳粒组成,每个壳粒含有病毒核酸编码的四种壳蛋白VP1~VP4,在5ˊ端结合一个病毒基因蛋白Vpg,在Vpg之后接着一段长约740 bp的非编码区,柯萨奇病毒按照在乳鼠中病变的不同而分为A,B两组,A组原有24个血清型,其中第23型后来被划归艾柯病毒9型,尚存23个血清型,这些血清型皆可用中和试验和补体结合试验加以区别,A组病毒虽不具有共同的抗原,但有型间的交叉免疫性,如A3和A8,A11和A15,A13和A18之间可有交叉血清反应;相反,在6个B组病毒的血清型和A9之间,则有共同的群抗原,除少数毒株外,柯萨奇病毒不产生红细胞凝集素,因而不能采用血凝抑制试验来鉴定。
柯萨奇病毒对新生小白鼠有高度致病性,A组病毒引起骨骼肌广泛性肌炎和弛缓性瘫痪而于1周内死亡,B组病毒可引起灶性分布的肌炎,并可引起脂肪组织炎,脑炎,心肌炎,胰腺炎,肝炎和心内膜炎,乳鼠常出现全身震颤,痉挛和强直性瘫痪。
较年长的小白鼠可耐受B组病毒感染,但可通过使用肾上腺皮质激素而诱发胰腺炎,营养不良可使B3病毒在成年小白鼠中产生严重疾病,包括在心,脾,肝,脑中的持续性感染,淋巴组织萎缩,将有免疫力的小白鼠淋巴细胞转移至营养不良小白鼠体内,可保护该小白鼠抵抗B3病毒,防止严重后果的产生。
A7,A9和A16病毒亦可在猴肾细胞培养中生长,某些A组毒株可在人羊膜细胞,Hela细胞或RD细胞株中生长,但A1,A19和A22病毒则未能在任何细胞培养中繁殖,血液中短暂出现,并通过粪便排出持续2~5周之久,A14病毒在成年小白鼠和猴子中引起脊髓灰质炎样病变,A7病毒在猴子中则引起严重中枢神经系统病变和瘫痪。
在细胞培养中,B组病毒可引起细胞病变,受染细胞变圆,皱缩,胞核固缩,反光,最后退化而脱落,A组病毒不产生细胞病变。
(二)发病机制
病毒由肠道或呼吸道进入人体后在小肠,咽部的上皮细胞及附近淋巴组织内繁殖复制,达一定程度后侵入血循环中,形成第1次(次要)病毒血症,此时患者可出现轻度不适或全无症状,病毒随血流进入各种靶组织,并在其中继续繁殖,导致组织细胞发生损害;同时再次侵入血循环(第2次或主要病毒血症),使各种靶组织又一次遭到病毒的侵袭,临床症状一般发生于组织细胞损害出现后及第2次病毒血症时。
在潜伏期的后一阶段或前驱期,并在此后的1周左右,病毒可自咽洗液或咽拭中被分离出,自粪便或肛拭中分离出病毒的时期则较长,可达2周至1个月之久,少数病例甚至在病后70天仍呈阳性;患病后的第1周的阳性率最高,以后逐渐下降,病毒还可以从患者的脑脊液,疱浆液,血液,尿,胸腔积液,心包液,骨髓等处检出,在死亡者的各种脏器如心,脑,肝,脾,肾,睾丸,肌肉等中也可分离到病毒。
病毒在体内的不断繁殖复制使人体产生一种具有抑制病毒复制的干扰素,当干扰素及特异性中和抗体在血中出现时,病毒即自血循环中消失,唾液及肠分泌物中的分泌型IgA是各种免疫球蛋白中最早出现者,有阻抑病毒自消化道侵入体内的作用,继而在血中出现IgM,自病程第1周起迅速上升,而于3~4周内下降或消失,IgG型中和抗体于感染后7~14天出现,3~4周内达高峰,并可维持多年,补体结合抗体与中和抗体同时出现,但仅维持2~3个月。
部分柯萨奇病毒经呼吸道进入人体仅引起上呼吸道感染而无病毒血症,病毒局限于呼吸道黏膜表面,并随着呼吸道分泌物而排出,粪便中无病毒。
组织损伤主要通过病毒在细胞内复制产生抑制因子,抑制细胞核糖核酸和蛋白质合成,而导致细胞破坏,但在某些肠道病毒中,免疫应答引起的组织损伤可能是疾病迁延的原因,如在心肌炎时早期组织损伤可能由病毒复制引起,后期病变则与免疫应答有关。
柯萨奇和埃可病毒所引起的中枢神经系统病变与脊髓灰质炎病毒所引起的病变相似,但柯萨奇B组病毒则同时可引起灰质和白质的病变,在婴儿中,常累及脑干。
柯萨奇B组病毒引起的心肌炎表现为间质的单核细胞浸润,伴有一定程度的水肿和心肌纤维坏死,左心室扩张及肥厚,部分病例有心包炎,偶可引起心内膜炎,心包炎通常为纤维素性,但也有渗出性的,心内膜肉眼可见心瓣膜游离,边缘有疣状突出,镜下为致密纤维组织及慢性炎症细胞浸润。
(一)发病原因
柯萨奇病毒属于小核糖核酸病毒科的肠道病毒属,病毒颗粒为球形或卵圆形,直径为22~30nm,呈圆形颗粒状,病毒基因组为单股线状RNA,全长约6000~8500 bp,构成病毒核心,外壳呈20面体,立体对称,由32个壳粒组成,每个壳粒含有病毒核酸编码的四种壳蛋白VP1~VP4,在5ˊ端结合一个病毒基因蛋白Vpg,在Vpg之后接着一段长约740 bp的非编码区,柯萨奇病毒按照在乳鼠中病变的不同而分为A,B两组,A组原有24个血清型,其中第23型后来被划归艾柯病毒9型,尚存23个血清型,这些血清型皆可用中和试验和补体结合试验加以区别,A组病毒虽不具有共同的抗原,但有型间的交叉免疫性,如A3和A8,A11和A15,A13和A18之间可有交叉血清反应;相反,在6个B组病毒的血清型和A9之间,则有共同的群抗原,除少数毒株外,柯萨奇病毒不产生红细胞凝集素,因而不能采用血凝抑制试验来鉴定。
柯萨奇病毒对新生小白鼠有高度致病性,A组病毒引起骨骼肌广泛性肌炎和弛缓性瘫痪而于1周内死亡,B组病毒可引起灶性分布的肌炎,并可引起脂肪组织炎,脑炎,心肌炎,胰腺炎,肝炎和心内膜炎,乳鼠常出现全身震颤,痉挛和强直性瘫痪。
较年长的小白鼠可耐受B组病毒感染,但可通过使用肾上腺皮质激素而诱发胰腺炎,营养不良可使B3病毒在成年小白鼠中产生严重疾病,包括在心,脾,肝,脑中的持续性感染,淋巴组织萎缩,将有免疫力的小白鼠淋巴细胞转移至营养不良小白鼠体内,可保护该小白鼠抵抗B3病毒,防止严重后果的产生。
A7,A9和A16病毒亦可在猴肾细胞培养中生长,某些A组毒株可在人羊膜细胞,Hela细胞或RD细胞株中生长,但A1,A19和A22病毒则未能在任何细胞培养中繁殖,血液中短暂出现,并通过粪便排出持续2~5周之久,A14病毒在成年小白鼠和猴子中引起脊髓灰质炎样病变,A7病毒在猴子中则引起严重中枢神经系统病变和瘫痪。
在细胞培养中,B组病毒可引起细胞病变,受染细胞变圆,皱缩,胞核固缩,反光,最后退化而脱落,A组病毒不产生细胞病变。
(二)发病机制
病毒由肠道或呼吸道进入人体后在小肠,咽部的上皮细胞及附近淋巴组织内繁殖复制,达一定程度后侵入血循环中,形成第1次(次要)病毒血症,此时患者可出现轻度不适或全无症状,病毒随血流进入各种靶组织,并在其中继续繁殖,导致组织细胞发生损害;同时再次侵入血循环(第2次或主要病毒血症),使各种靶组织又一次遭到病毒的侵袭,临床症状一般发生于组织细胞损害出现后及第2次病毒血症时。
在潜伏期的后一阶段或前驱期,并在此后的1周左右,病毒可自咽洗液或咽拭中被分离出,自粪便或肛拭中分离出病毒的时期则较长,可达2周至1个月之久,少数病例甚至在病后70天仍呈阳性;患病后的第1周的阳性率最高,以后逐渐下降,病毒还可以从患者的脑脊液,疱浆液,血液,尿,胸腔积液,心包液,骨髓等处检出,在死亡者的各种脏器如心,脑,肝,脾,肾,睾丸,肌肉等中也可分离到病毒。
病毒在体内的不断繁殖复制使人体产生一种具有抑制病毒复制的干扰素,当干扰素及特异性中和抗体在血中出现时,病毒即自血循环中消失,唾液及肠分泌物中的分泌型IgA是各种免疫球蛋白中最早出现者,有阻抑病毒自消化道侵入体内的作用,继而在血中出现IgM,自病程第1周起迅速上升,而于3~4周内下降或消失,IgG型中和抗体于感染后7~14天出现,3~4周内达高峰,并可维持多年,补体结合抗体与中和抗体同时出现,但仅维持2~3个月。
部分柯萨奇病毒经呼吸道进入人体仅引起上呼吸道感染而无病毒血症,病毒局限于呼吸道黏膜表面,并随着呼吸道分泌物而排出,粪便中无病毒。
组织损伤主要通过病毒在细胞内复制产生抑制因子,抑制细胞核糖核酸和蛋白质合成,而导致细胞破坏,但在某些肠道病毒中,免疫应答引起的组织损伤可能是疾病迁延的原因,如在心肌炎时早期组织损伤可能由病毒复制引起,后期病变则与免疫应答有关。
柯萨奇和埃可病毒所引起的中枢神经系统病变与脊髓灰质炎病毒所引起的病变相似,但柯萨奇B组病毒则同时可引起灰质和白质的病变,在婴儿中,常累及脑干。
柯萨奇B组病毒引起的心肌炎表现为间质的单核细胞浸润,伴有一定程度的水肿和心肌纤维坏死,左心室扩张及肥厚,部分病例有心包炎,偶可引起心内膜炎,心包炎通常为纤维素性,但也有渗出性的,心内膜肉眼可见心瓣膜游离,边缘有疣状突出,镜下为致密纤维组织及慢性炎症细胞浸润。
(一)发病原因
柯萨奇病毒属于小核糖核酸病毒科的肠道病毒属,病毒颗粒为球形或卵圆形,直径为22~30nm,呈圆形颗粒状,病毒基因组为单股线状RNA,全长约6000~8500 bp,构成病毒核心,外壳呈20面体,立体对称,由32个壳粒组成,每个壳粒含有病毒核酸编码的四种壳蛋白VP1~VP4,在5ˊ端结合一个病毒基因蛋白Vpg,在Vpg之后接着一段长约740 bp的非编码区,柯萨奇病毒按照在乳鼠中病变的不同而分为A,B两组,A组原有24个血清型,其中第23型后来被划归艾柯病毒9型,尚存23个血清型,这些血清型皆可用中和试验和补体结合试验加以区别,A组病毒虽不具有共同的抗原,但有型间的交叉免疫性,如A3和A8,A11和A15,A13和A18之间可有交叉血清反应;相反,在6个B组病毒的血清型和A9之间,则有共同的群抗原,除少数毒株外,柯萨奇病毒不产生红细胞凝集素,因而不能采用血凝抑制试验来鉴定。
柯萨奇病毒对新生小白鼠有高度致病性,A组病毒引起骨骼肌广泛性肌炎和弛缓性瘫痪而于1周内死亡,B组病毒可引起灶性分布的肌炎,并可引起脂肪组织炎,脑炎,心肌炎,胰腺炎,肝炎和心内膜炎,乳鼠常出现全身震颤,痉挛和强直性瘫痪。
较年长的小白鼠可耐受B组病毒感染,但可通过使用肾上腺皮质激素而诱发胰腺炎,营养不良可使B3病毒在成年小白鼠中产生严重疾病,包括在心,脾,肝,脑中的持续性感染,淋巴组织萎缩,将有免疫力的小白鼠淋巴细胞转移至营养不良小白鼠体内,可保护该小白鼠抵抗B3病毒,防止严重后果的产生。
A7,A9和A16病毒亦可在猴肾细胞培养中生长,某些A组毒株可在人羊膜细胞,Hela细胞或RD细胞株中生长,但A1,A19和A22病毒则未能在任何细胞培养中繁殖,血液中短暂出现,并通过粪便排出持续2~5周之久,A14病毒在成年小白鼠和猴子中引起脊髓灰质炎样病变,A7病毒在猴子中则引起严重中枢神经系统病变和瘫痪。
在细胞培养中,B组病毒可引起细胞病变,受染细胞变圆,皱缩,胞核固缩,反光,最后退化而脱落,A组病毒不产生细胞病变。
(二)发病机制
病毒由肠道或呼吸道进入人体后在小肠,咽部的上皮细胞及附近淋巴组织内繁殖复制,达一定程度后侵入血循环中,形成第1次(次要)病毒血症,此时患者可出现轻度不适或全无症状,病毒随血流进入各种靶组织,并在其中继续繁殖,导致组织细胞发生损害;同时再次侵入血循环(第2次或主要病毒血症),使各种靶组织又一次遭到病毒的侵袭,临床症状一般发生于组织细胞损害出现后及第2次病毒血症时。
在潜伏期的后一阶段或前驱期,并在此后的1周左右,病毒可自咽洗液或咽拭中被分离出,自粪便或肛拭中分离出病毒的时期则较长,可达2周至1个月之久,少数病例甚至在病后70天仍呈阳性;患病后的第1周的阳性率最高,以后逐渐下降,病毒还可以从患者的脑脊液,疱浆液,血液,尿,胸腔积液,心包液,骨髓等处检出,在死亡者的各种脏器如心,脑,肝,脾,肾,睾丸,肌肉等中也可分离到病毒。
病毒在体内的不断繁殖复制使人体产生一种具有抑制病毒复制的干扰素,当干扰素及特异性中和抗体在血中出现时,病毒即自血循环中消失,唾液及肠分泌物中的分泌型IgA是各种免疫球蛋白中最早出现者,有阻抑病毒自消化道侵入体内的作用,继而在血中出现IgM,自病程第1周起迅速上升,而于3~4周内下降或消失,IgG型中和抗体于感染后7~14天出现,3~4周内达高峰,并可维持多年,补体结合抗体与中和抗体同时出现,但仅维持2~3个月。
部分柯萨奇病毒经呼吸道进入人体仅引起上呼吸道感染而无病毒血症,病毒局限于呼吸道黏膜表面,并随着呼吸道分泌物而排出,粪便中无病毒。
组织损伤主要通过病毒在细胞内复制产生抑制因子,抑制细胞核糖核酸和蛋白质合成,而导致细胞破坏,但在某些肠道病毒中,免疫应答引起的组织损伤可能是疾病迁延的原因,如在心肌炎时早期组织损伤可能由病毒复制引起,后期病变则与免疫应答有关。
柯萨奇和埃可病毒所引起的中枢神经系统病变与脊髓灰质炎病毒所引起的病变相似,但柯萨奇B组病毒则同时可引起灰质和白质的病变,在婴儿中,常累及脑干。
柯萨奇B组病毒引起的心肌炎表现为间质的单核细胞浸润,伴有一定程度的水肿和心肌纤维坏死,左心室扩张及肥厚,部分病例有心包炎,偶可引起心内膜炎,心包炎通常为纤维素性,但也有渗出性的,心内膜肉眼可见心瓣膜游离,边缘有疣状突出,镜下为致密纤维组织及慢性炎症细胞浸润。
(一)发病原因
柯萨奇病毒属于小核糖核酸病毒科的肠道病毒属,病毒颗粒为球形或卵圆形,直径为22~30nm,呈圆形颗粒状,病毒基因组为单股线状RNA,全长约6000~8500 bp,构成病毒核心,外壳呈20面体,立体对称,由32个壳粒组成,每个壳粒含有病毒核酸编码的四种壳蛋白VP1~VP4,在5ˊ端结合一个病毒基因蛋白Vpg,在Vpg之后接着一段长约740 bp的非编码区,柯萨奇病毒按照在乳鼠中病变的不同而分为A,B两组,A组原有24个血清型,其中第23型后来被划归艾柯病毒9型,尚存23个血清型,这些血清型皆可用中和试验和补体结合试验加以区别,A组病毒虽不具有共同的抗原,但有型间的交叉免疫性,如A3和A8,A11和A15,A13和A18之间可有交叉血清反应;相反,在6个B组病毒的血清型和A9之间,则有共同的群抗原,除少数毒株外,柯萨奇病毒不产生红细胞凝集素,因而不能采用血凝抑制试验来鉴定。
柯萨奇病毒对新生小白鼠有高度致病性,A组病毒引起骨骼肌广泛性肌炎和弛缓性瘫痪而于1周内死亡,B组病毒可引起灶性分布的肌炎,并可引起脂肪组织炎,脑炎,心肌炎,胰腺炎,肝炎和心内膜炎,乳鼠常出现全身震颤,痉挛和强直性瘫痪。
较年长的小白鼠可耐受B组病毒感染,但可通过使用肾上腺皮质激素而诱发胰腺炎,营养不良可使B3病毒在成年小白鼠中产生严重疾病,包括在心,脾,肝,脑中的持续性感染,淋巴组织萎缩,将有免疫力的小白鼠淋巴细胞转移至营养不良小白鼠体内,可保护该小白鼠抵抗B3病毒,防止严重后果的产生。
A7,A9和A16病毒亦可在猴肾细胞培养中生长,某些A组毒株可在人羊膜细胞,Hela细胞或RD细胞株中生长,但A1,A19和A22病毒则未能在任何细胞培养中繁殖,血液中短暂出现,并通过粪便排出持续2~5周之久,A14病毒在成年小白鼠和猴子中引起脊髓灰质炎样病变,A7病毒在猴子中则引起严重中枢神经系统病变和瘫痪。
在细胞培养中,B组病毒可引起细胞病变,受染细胞变圆,皱缩,胞核固缩,反光,最后退化而脱落,A组病毒不产生细胞病变。
(二)发病机制
病毒由肠道或呼吸道进入人体后在小肠,咽部的上皮细胞及附近淋巴组织内繁殖复制,达一定程度后侵入血循环中,形成第1次(次要)病毒血症,此时患者可出现轻度不适或全无症状,病毒随血流进入各种靶组织,并在其中继续繁殖,导致组织细胞发生损害;同时再次侵入血循环(第2次或主要病毒血症),使各种靶组织又一次遭到病毒的侵袭,临床症状一般发生于组织细胞损害出现后及第2次病毒血症时。
在潜伏期的后一阶段或前驱期,并在此后的1周左右,病毒可自咽洗液或咽拭中被分离出,自粪便或肛拭中分离出病毒的时期则较长,可达2周至1个月之久,少数病例甚至在病后70天仍呈阳性;患病后的第1周的阳性率最高,以后逐渐下降,病毒还可以从患者的脑脊液,疱浆液,血液,尿,胸腔积液,心包液,骨髓等处检出,在死亡者的各种脏器如心,脑,肝,脾,肾,睾丸,肌肉等中也可分离到病毒。
病毒在体内的不断繁殖复制使人体产生一种具有抑制病毒复制的干扰素,当干扰素及特异性中和抗体在血中出现时,病毒即自血循环中消失,唾液及肠分泌物中的分泌型IgA是各种免疫球蛋白中最早出现者,有阻抑病毒自消化道侵入体内的作用,继而在血中出现IgM,自病程第1周起迅速上升,而于3~4周内下降或消失,IgG型中和抗体于感染后7~14天出现,3~4周内达高峰,并可维持多年,补体结合抗体与中和抗体同时出现,但仅维持2~3个月。
部分柯萨奇病毒经呼吸道进入人体仅引起上呼吸道感染而无病毒血症,病毒局限于呼吸道黏膜表面,并随着呼吸道分泌物而排出,粪便中无病毒。
组织损伤主要通过病毒在细胞内复制产生抑制因子,抑制细胞核糖核酸和蛋白质合成,而导致细胞破坏,但在某些肠道病毒中,免疫应答引起的组织损伤可能是疾病迁延的原因,如在心肌炎时早期组织损伤可能由病毒复制引起,后期病变则与免疫应答有关。
柯萨奇和埃可病毒所引起的中枢神经系统病变与脊髓灰质炎病毒所引起的病变相似,但柯萨奇B组病毒则同时可引起灰质和白质的病变,在婴儿中,常累及脑干。
柯萨奇B组病毒引起的心肌炎表现为间质的单核细胞浸润,伴有一定程度的水肿和心肌纤维坏死,左心室扩张及肥厚,部分病例有心包炎,偶可引起心内膜炎,心包炎通常为纤维素性,但也有渗出性的,心内膜肉眼可见心瓣膜游离,边缘有疣状突出,镜下为致密纤维组织及慢性炎症细胞浸润。
(一)发病原因
柯萨奇病毒属于小核糖核酸病毒科的肠道病毒属,病毒颗粒为球形或卵圆形,直径为22~30nm,呈圆形颗粒状,病毒基因组为单股线状RNA,全长约6000~8500 bp,构成病毒核心,外壳呈20面体,立体对称,由32个壳粒组成,每个壳粒含有病毒核酸编码的四种壳蛋白VP1~VP4,在5ˊ端结合一个病毒基因蛋白Vpg,在Vpg之后接着一段长约740 bp的非编码区,柯萨奇病毒按照在乳鼠中病变的不同而分为A,B两组,A组原有24个血清型,其中第23型后来被划归艾柯病毒9型,尚存23个血清型,这些血清型皆可用中和试验和补体结合试验加以区别,A组病毒虽不具有共同的抗原,但有型间的交叉免疫性,如A3和A8,A11和A15,A13和A18之间可有交叉血清反应;相反,在6个B组病毒的血清型和A9之间,则有共同的群抗原,除少数毒株外,柯萨奇病毒不产生红细胞凝集素,因而不能采用血凝抑制试验来鉴定。
柯萨奇病毒对新生小白鼠有高度致病性,A组病毒引起骨骼肌广泛性肌炎和弛缓性瘫痪而于1周内死亡,B组病毒可引起灶性分布的肌炎,并可引起脂肪组织炎,脑炎,心肌炎,胰腺炎,肝炎和心内膜炎,乳鼠常出现全身震颤,痉挛和强直性瘫痪。
较年长的小白鼠可耐受B组病毒感染,但可通过使用肾上腺皮质激素而诱发胰腺炎,营养不良可使B3病毒在成年小白鼠中产生严重疾病,包括在心,脾,肝,脑中的持续性感染,淋巴组织萎缩,将有免疫力的小白鼠淋巴细胞转移至营养不良小白鼠体内,可保护该小白鼠抵抗B3病毒,防止严重后果的产生。
A7,A9和A16病毒亦可在猴肾细胞培养中生长,某些A组毒株可在人羊膜细胞,Hela细胞或RD细胞株中生长,但A1,A19和A22病毒则未能在任何细胞培养中繁殖,血液中短暂出现,并通过粪便排出持续2~5周之久,A14病毒在成年小白鼠和猴子中引起脊髓灰质炎样病变,A7病毒在猴子中则引起严重中枢神经系统病变和瘫痪。
在细胞培养中,B组病毒可引起细胞病变,受染细胞变圆,皱缩,胞核固缩,反光,最后退化而脱落,A组病毒不产生细胞病变。
(二)发病机制
病毒由肠道或呼吸道进入人体后在小肠,咽部的上皮细胞及附近淋巴组织内繁殖复制,达一定程度后侵入血循环中,形成第1次(次要)病毒血症,此时患者可出现轻度不适或全无症状,病毒随血流进入各种靶组织,并在其中继续繁殖,导致组织细胞发生损害;同时再次侵入血循环(第2次或主要病毒血症),使各种靶组织又一次遭到病毒的侵袭,临床症状一般发生于组织细胞损害出现后及第2次病毒血症时。
在潜伏期的后一阶段或前驱期,并在此后的1周左右,病毒可自咽洗液或咽拭中被分离出,自粪便或肛拭中分离出病毒的时期则较长,可达2周至1个月之久,少数病例甚至在病后70天仍呈阳性;患病后的第1周的阳性率最高,以后逐渐下降,病毒还可以从患者的脑脊液,疱浆液,血液,尿,胸腔积液,心包液,骨髓等处检出,在死亡者的各种脏器如心,脑,肝,脾,肾,睾丸,肌肉等中也可分离到病毒。
病毒在体内的不断繁殖复制使人体产生一种具有抑制病毒复制的干扰素,当干扰素及特异性中和抗体在血中出现时,病毒即自血循环中消失,唾液及肠分泌物中的分泌型IgA是各种免疫球蛋白中最早出现者,有阻抑病毒自消化道侵入体内的作用,继而在血中出现IgM,自病程第1周起迅速上升,而于3~4周内下降或消失,IgG型中和抗体于感染后7~14天出现,3~4周内达高峰,并可维持多年,补体结合抗体与中和抗体同时出现,但仅维持2~3个月。
部分柯萨奇病毒经呼吸道进入人体仅引起上呼吸道感染而无病毒血症,病毒局限于呼吸道黏膜表面,并随着呼吸道分泌物而排出,粪便中无病毒。
组织损伤主要通过病毒在细胞内复制产生抑制因子,抑制细胞核糖核酸和蛋白质合成,而导致细胞破坏,但在某些肠道病毒中,免疫应答引起的组织损伤可能是疾病迁延的原因,如在心肌炎时早期组织损伤可能由病毒复制引起,后期病变则与免疫应答有关。
柯萨奇和埃可病毒所引起的中枢神经系统病变与脊髓灰质炎病毒所引起的病变相似,但柯萨奇B组病毒则同时可引起灰质和白质的病变,在婴儿中,常累及脑干。
柯萨奇B组病毒引起的心肌炎表现为间质的单核细胞浸润,伴有一定程度的水肿和心肌纤维坏死,左心室扩张及肥厚,部分病例有心包炎,偶可引起心内膜炎,心包炎通常为纤维素性,但也有渗出性的,心内膜肉眼可见心瓣膜游离,边缘有疣状突出,镜下为致密纤维组织及慢性炎症细胞浸润。
(一)发病原因
柯萨奇病毒属于小核糖核酸病毒科的肠道病毒属,病毒颗粒为球形或卵圆形,直径为22~30nm,呈圆形颗粒状,病毒基因组为单股线状RNA,全长约6000~8500 bp,构成病毒核心,外壳呈20面体,立体对称,由32个壳粒组成,每个壳粒含有病毒核酸编码的四种壳蛋白VP1~VP4,在5ˊ端结合一个病毒基因蛋白Vpg,在Vpg之后接着一段长约740 bp的非编码区,柯萨奇病毒按照在乳鼠中病变的不同而分为A,B两组,A组原有24个血清型,其中第23型后来被划归艾柯病毒9型,尚存23个血清型,这些血清型皆可用中和试验和补体结合试验加以区别,A组病毒虽不具有共同的抗原,但有型间的交叉免疫性,如A3和A8,A11和A15,A13和A18之间可有交叉血清反应;相反,在6个B组病毒的血清型和A9之间,则有共同的群抗原,除少数毒株外,柯萨奇病毒不产生红细胞凝集素,因而不能采用血凝抑制试验来鉴定。
柯萨奇病毒对新生小白鼠有高度致病性,A组病毒引起骨骼肌广泛性肌炎和弛缓性瘫痪而于1周内死亡,B组病毒可引起灶性分布的肌炎,并可引起脂肪组织炎,脑炎,心肌炎,胰腺炎,肝炎和心内膜炎,乳鼠常出现全身震颤,痉挛和强直性瘫痪。
较年长的小白鼠可耐受B组病毒感染,但可通过使用肾上腺皮质激素而诱发胰腺炎,营养不良可使B3病毒在成年小白鼠中产生严重疾病,包括在心,脾,肝,脑中的持续性感染,淋巴组织萎缩,将有免疫力的小白鼠淋巴细胞转移至营养不良小白鼠体内,可保护该小白鼠抵抗B3病毒,防止严重后果的产生。
A7,A9和A16病毒亦可在猴肾细胞培养中生长,某些A组毒株可在人羊膜细胞,Hela细胞或RD细胞株中生长,但A1,A19和A22病毒则未能在任何细胞培养中繁殖,血液中短暂出现,并通过粪便排出持续2~5周之久,A14病毒在成年小白鼠和猴子中引起脊髓灰质炎样病变,A7病毒在猴子中则引起严重中枢神经系统病变和瘫痪。
在细胞培养中,B组病毒可引起细胞病变,受染细胞变圆,皱缩,胞核固缩,反光,最后退化而脱落,A组病毒不产生细胞病变。
(二)发病机制
病毒由肠道或呼吸道进入人体后在小肠,咽部的上皮细胞及附近淋巴组织内繁殖复制,达一定程度后侵入血循环中,形成第1次(次要)病毒血症,此时患者可出现轻度不适或全无症状,病毒随血流进入各种靶组织,并在其中继续繁殖,导致组织细胞发生损害;同时再次侵入血循环(第2次或主要病毒血症),使各种靶组织又一次遭到病毒的侵袭,临床症状一般发生于组织细胞损害出现后及第2次病毒血症时。
在潜伏期的后一阶段或前驱期,并在此后的1周左右,病毒可自咽洗液或咽拭中被分离出,自粪便或肛拭中分离出病毒的时期则较长,可达2周至1个月之久,少数病例甚至在病后70天仍呈阳性;患病后的第1周的阳性率最高,以后逐渐下降,病毒还可以从患者的脑脊液,疱浆液,血液,尿,胸腔积液,心包液,骨髓等处检出,在死亡者的各种脏器如心,脑,肝,脾,肾,睾丸,肌肉等中也可分离到病毒。
病毒在体内的不断繁殖复制使人体产生一种具有抑制病毒复制的干扰素,当干扰素及特异性中和抗体在血中出现时,病毒即自血循环中消失,唾液及肠分泌物中的分泌型IgA是各种免疫球蛋白中最早出现者,有阻抑病毒自消化道侵入体内的作用,继而在血中出现IgM,自病程第1周起迅速上升,而于3~4周内下降或消失,IgG型中和抗体于感染后7~14天出现,3~4周内达高峰,并可维持多年,补体结合抗体与中和抗体同时出现,但仅维持2~3个月。
部分柯萨奇病毒经呼吸道进入人体仅引起上呼吸道感染而无病毒血症,病毒局限于呼吸道黏膜表面,并随着呼吸道分泌物而排出,粪便中无病毒。
组织损伤主要通过病毒在细胞内复制产生抑制因子,抑制细胞核糖核酸和蛋白质合成,而导致细胞破坏,但在某些肠道病毒中,免疫应答引起的组织损伤可能是疾病迁延的原因,如在心肌炎时早期组织损伤可能由病毒复制引起,后期病变则与免疫应答有关。
柯萨奇和埃可病毒所引起的中枢神经系统病变与脊髓灰质炎病毒所引起的病变相似,但柯萨奇B组病毒则同时可引起灰质和白质的病变,在婴儿中,常累及脑干。
柯萨奇B组病毒引起的心肌炎表现为间质的单核细胞浸润,伴有一定程度的水肿和心肌纤维坏死,左心室扩张及肥厚,部分病例有心包炎,偶可引起心内膜炎,心包炎通常为纤维素性,但也有渗出性的,心内膜肉眼可见心瓣膜游离,边缘有疣状突出,镜下为致密纤维组织及慢性炎症细胞浸润。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。