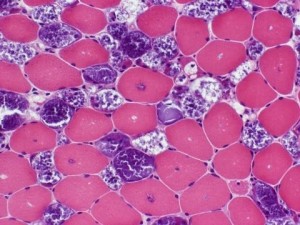
小儿糖原贮积病Ⅱ型
疾病概述
糖原贮积病是由于遗传性糖原代谢障碍,致使糖原在组织内过多沉积而引起的疾病。糖原贮积病Ⅱ型(Pompe 病)又称酸性麦芽糖酶缺陷病。本病属常染色体隐性遗传,也可散发。临床可分婴儿型、儿童型和成人型。
1.婴儿型 常在出生1 个月或3~4 个月后发病。首发症状为进食后发绀,呼吸困难,呼吸窘迫。全身肌肉无力,呈弛缓性瘫痪,且病情进展较快,常在1 岁之内死亡。检查可见巨舌,心脏扩大,少数病儿肝脏肿大,心律失常。
2.儿童型 以四肢无力为主要临床表现,类似肢带型肌营养不良症。常有呼吸困难、发绀,心脏扩大、心力衰竭及腓肠肌肥大。
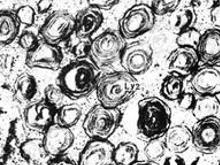 3.成人型 30~40 岁发病,缓慢进展性的四肢肌肉萎缩、无力,近端较远端重。以躯干肌、骨盆带肌明显,半数以上病人影响呼吸肌。常被误诊为多发性肌炎或肌营养不良症。预后较好。
3.成人型 30~40 岁发病,缓慢进展性的四肢肌肉萎缩、无力,近端较远端重。以躯干肌、骨盆带肌明显,半数以上病人影响呼吸肌。常被误诊为多发性肌炎或肌营养不良症。预后较好。
病理病因
病因
本病属常染色体隐性遗传也可散发。本病编码酸性麦芽糖酶的基因定位于17号染色体长臂23区(17q23)。Ⅱ型糖原贮积症是由于常染色体上的一个隐性基因突变,造成α-l,4-葡糖苷酶(酸性麦芽糖酶)(acid maltase deficiency,AMD)缺乏所致,麦芽糖酶是一溶酶体酶,包括酸性和中性麦芽糖酶两种,分解α-1、4 糖苷键和α-1、6 糖苷键而游离葡萄糖分子能使低聚糖和糖原分解出葡萄糖,酶缺乏时,缺少了这种酶的溶酶体不能把肝细胞中或肝细胞中过剩的糖原进行水解而大量积累在溶酶体内,造成溶酶体超载。大量糖原累积在溶酶体内,溶酶体膨胀造成细胞受损。体内各种组织均受累,心肌和骨骼肌有糖原沉积,影响了心脏的收缩功能而产生心力衰竭。病理检查可见肝、肌肉、心、脑干运动核和脊髓前角细胞中有大量糖原累积。糖原贮积病Ⅱ型的神经系统表现主要是运动障碍,以四肢肌无力、肌萎缩、假性肥大等肌病表现多见。溶酶体外的糖原代谢正常。根据引起糖原代谢障碍的酶缺陷和过量糖原在体内沉积的组织不同,而将糖原贮积病分为11 种类型。
1.0 型 尿二磷葡萄糖-糖原转移酶缺陷。临床表现为肝大、低血糖、先天性肌无力,肌张力减低。
2.Ⅰ型 葡萄糖-6-膦酸酯酶缺陷。临床表现为肝大、低血糖、酮中毒、酸中毒。
3.Ⅱ型 α-1,4-糖苷酶缺陷。心脏增大、心力衰竭、巨舌,肌无力。
4.Ⅲ型 多糖-1,6-糖苷酶和(或)果糖-1,4→1,4-转葡萄糖苷酶缺陷。临床表现为肝大、低血糖、先天性肌无力,肌张力减低。
5.Ⅳ型 多糖-1,4→1,6-转葡萄糖苷酶缺陷。临床表现为肝、脾大,肝硬化。
6.Ⅴ型 肌肉磷酸化酶缺陷。临床表现为运动后肌肉疼痛,无力。
8.Ⅶ型 磷酸果糖激酶缺陷。临床表现为运动后肌肉疼痛,无力。
9.Ⅷ型 磷酸己糖异构酶缺陷。临床表现为运动后肌肉疼痛,无力。
11.Ⅸb 型 磷酸化酶激酶缺陷。
12.Ⅹ型 磷酸化酶激酶缺陷。临床表现为运动后肌肉疼痛,无力。
发病机制
糖原贮积病Ⅱ型(GSD-Ⅱ)是由于α-1,4-葡萄糖苷酶(酸性麦芽糖酶)缺陷所致,该酶属溶酶体酶,其作用是使低聚糖和糖原分解成葡萄糖;酶缺乏时即导致大量糖原贮积在溶酶体中,溶酶体膨胀造成细胞损伤。由此肌糖原的分解发生障碍,心肌和骨骼肌有糖原沉积,心肌因含大量的糖原呈夹板状,因此影响了心脏的收缩功能而产生心力衰竭。
临床分类
糖原贮积病是由于遗传性糖原代谢障碍,致使糖原在组织内过多沉积而引起的疾病。根据引起糖原代谢障碍的酶缺陷和过量糖原在体内沉积的组织不同,而将糖原贮积病分为11 种类型。
糖原贮积病Ⅱ型(Pompe 病)又称酸性麦芽糖酶缺陷病。本病属常染色体隐性遗传,也可散发。临床可分婴儿型、儿童型和成人型。糖原贮积病Ⅱ型(Pompe病),由酸性麦芽糖酶(acid maltase deficiency,AMD)缺乏而引起糖原在溶酶体内沉积、溶酶体增生、破坏,甚至释放不正常的溶酶体酶而致一系列的血细胞结构破坏。糖原贮积病Ⅱ型的神经系统表现主要是运动障碍,以四肢肌无力、肌萎缩、假性肥大等肌病表现多见。
糖原贮积病的分类:
1.0 型 尿二磷葡萄糖-糖原转移酶缺陷。临床表现为肝大、低血糖、先天性肌无力,肌张力减低。
2.Ⅰ型 葡萄糖-6-膦酸酯酶缺陷。临床表现为肝大、低血糖、酮中毒、酸中毒。
3.Ⅱ型 α-1,4-糖苷酶缺陷。心脏增大、心力衰竭、巨舌,肌无力。
4.Ⅲ型 多糖-1,6-糖苷酶和(或)果糖-1,4→1,4-转葡萄糖苷酶缺陷。临床表现为肝大、低血糖、先天性肌无力,肌张力减低。
5.Ⅳ型 多糖-1,4→1,6-转葡萄糖苷酶缺陷。临床表现为肝、脾大,肝硬化。
6.Ⅴ型 肌肉磷酸化酶缺陷。临床表现为运动后肌肉疼痛,无力。
8.Ⅶ型 磷酸果糖激酶缺陷。临床表现为运动后肌肉疼痛,无力。
9.Ⅷ型 磷酸己糖异构酶缺陷。临床表现为运动后肌肉疼痛,无力。
11.Ⅸb 型 磷酸化酶激酶缺陷。
症状体征
Ⅱ型糖原累积病的总发病率约为1/4万,各亚型的发病率有地区差异性:婴儿型在非裔美国人和中国人中的发病率明显高于其他国家;而成人型在荷兰人中的发病率较高。 本病按发病年龄、病变累及的主要器官和病情轻重分为3型:婴儿型、幼儿型、成人型。个型的主要特征和诊断依据(心脏和肌肉的体征具典型诊断依据)为:
1.婴儿型:娩出时正常,多在新生儿期发病,也可生后数月出现症状。表现为食欲不振、喂养困难、呕吐、生长发育缓慢,随之出现呼吸困难、青紫、烦躁、咳嗽及水肿等功能不全症状。并表现有全身性的严重肌张力低下(软婴状)、自发运动减少为特征。4~5个月时腱反射消失。进行性衰弱,几乎呈完全性弛缓性瘫痪。咽部唾液壅塞,咳无力,呼吸浅易发生肺炎。常见巨舌、不同程度心肥大,可有充血性心力衰竭。心电图显示高大QRS波和P-R间期缩短,T波倒置,ST段改变,肝中度肿大。血糖、血脂及酮体正常。患儿常在2岁以内死于心力衰竭或吸入性肺炎。可根据尿内酸性麦芽糖及中性麦芽糖缺乏确诊。
2.幼儿型:起病稍晚,在婴儿或幼儿期起病,病程进展较慢,除肌无力外,其他器官受累不一。常以动作发育迟滞或步态不稳为初起症状,继而肌力减退、吞咽困难、呼吸肌亦被侵及,心脏可增大,但少有心衰发生,患者常在20岁之前死于呼吸衰竭。可根据肌肉、肝脏、心脏、白细胞内酸性麦芽糖下降确诊。
3.成人型 多在20~70岁发病,30~40岁症状明显,表现为进展缓慢的全身性肌病,以下肢为最重,无心、肝等器官增大,有时可无症状。可根据肌肉、肝内酸性麦芽糖下降或消失而中性麦芽糖正常,或肌肉活组织检查,于切片中见到较多的糖原沉积,周围血白细胞的糖原染色阳性,予以肯定诊断。
【实验室检查】
用皮肤或纤维细胞,白细胞,肌细胞进行酶分析可确诊,肌活检可见糖原沉积,与其他各型糖原贮积病不同,葡萄糖耐量和糖原反应皆正常,无低血糖、酸中毒或酮中毒。
1.血生化检查
3.肌电图示强直电位活动,见肌纤颤电位,运动单位电位正常或时限缩短。运动神经传导速度正常。
4.肌活检 肌纤维出现大小不等的散在空泡。PAS 染色可见阳性颗粒。电子显微镜下:糖原沉积于肌壁上,肌原纤维内和吞噬性空泡内肌纤维稀少、肿胀。
并发病症
1.充血性心力衰竭:系指在有适量静脉血回流的情况下,由于心脏收缩和(或)舒张功能障碍,心排血量不足以维持组织代谢需要的一种病理状态。临床上根据病变的心脏和淤血部位,可分为左心、右心和全心心衰,其中以左心衰开始较多见,以后继发肺动脉高压,导致右心衰,单纯的右心衰较少见。
2.吸入性肺炎:系吸入酸性物质、动物脂肪如食物、胃容物以及其他刺激性液体和发挥性的碳氢化合物后,引起的化学性肺炎。严重者可发生呼吸衰竭或呼吸窘迫综合征。
3.呼吸衰竭:由各种原因导致严重呼吸功能障碍,引起动脉血氧分压(PaO2)降低,伴或不伴有动脉血二氧化碳分压(PaCO2)增高而出现一系列病理生理紊乱的临床综合征。它是一种功能障碍状态,而不是一种疾病,可因肺部疾病引起也可能是各种疾病的并发症。
4.肺炎:指终末气道、肺泡和肺间质的炎症,可由疾病微生物、理化因素、免疫损伤、过敏及药物所致。细菌性肺炎是最常见的肺炎,也是最常见的感染性疾病之一。日常所讲的肺炎主要是指细菌性感染引起的肺炎,此肺炎也是最常见的一种。在抗生素应用以前,细菌性肺炎对儿童及老年人额健康威胁极大,抗生素的出现及发展曾一度使肺炎病死率明显下降。但近年来,尽管应用强有力的抗生素和有效的疫苗,肺炎总的病死率不再降低,甚至有所上升。
检查鉴别
一、检查
1.血液检查:血清肌酸激酶、谷草转氨酶和乳酸脱氢酶活力增高;
2.肌电图:显示肌病特征。应用电子学仪器记录肌肉静止或收缩时的电活动,及应用电刺激检查神经、肌肉兴奋及传导功能的方法。英文简称EMG。通过此检查可以确定周围神经、神经元、神经肌肉接头及肌肉本身的功能状态;
3.肌肉活检:可见糖原贮积和酸性磷酸酶增高(表明溶酶体酶代偿加强)。确诊需依据肌活检组织或培养成纤维细胞的酶学检测;
5.心电图:显著电轴左偏,显示高大QRS波和P-R间期缩短,ST段下降,T波倒置。
6.羊水细胞或绒膜绒毛的酶学检测可供本病婴儿型的产前诊断。
7.GAA活性测定诊断法:帮助确诊Ⅱ型糖原累积病,损伤较小、操作简便。常用的方法是对取自皮肤活检的成纤维细胞进行培养,当培养到一定数量时对细胞内的GAA活性进行检测。但此过程需要4~6周,因此明显延迟了诊断。
8.干血斑(DBS)检测法:即检测干血斑提取物中的GAA活性。本方法是用指针法获取标本并置于滤纸上,然后运送到检测分析中心进行检测。然而,此法需用免疫捕获从干血斑提取物中分离GAA并用麦芽糖或阿卡波糖来竞争性抑制麦芽糖酶—葡萄糖淀粉酶(MGA)活性以去除MGA活性的干扰。这种新的干血斑方法不仅适用于新生儿Ⅱ型糖原累积病的筛查,还可作为快速无创的初步诊断性检查来排除Ⅱ型糖原累积病。该方法与尿Glc4水平检测法合用,对婴儿型Ⅱ型糖原累积病的诊断敏感性接近100%。而且,这两种检测方法得到的阴性结果基本可以排除婴儿型Ⅱ型糖原累积病。目前,用干血液过滤样本进行新生儿GAA活性的大批量筛查的方法已得到改进,而且此方法正在大量人口筛查项目中被验证是否有效。如果成功的话,对新生儿Ⅱ型糖原累积病进行筛查将会成为可能。
二、鉴别
1.先天性肌弛缓:以肌型为主要表现者应与先天性肌弛缓相鉴别。后者包括一组原因不同的先天性神经肌肉疾病。早在1900年欧本哈姆报道一种先天性疾病,出生时大多数肌肉的张力低下,腱反射消失,但无电流变性反应,当时认为是一个独立的病种。以后,同一家庭出现先天性肌弛缓和脊髓性进行性肌萎缩两种病例,认为此二病的病理完全相同,仅症状略异,此二病之间还出现中间病型。最后,公认欧本哈姆所叙述的先天性肌弛缓,是脊髓性进行性肌萎缩的轻型。良性先天性肌弛缓综合征即先天性肌张力不全症(congenital myodystony ),又称Oppenheim综合征、良性先天性肌病综合征等。本病征属先天性肌弛缓症中的一种较为良性的类型,以出生后婴儿期即有大多数肌肉张力减弱、肌无力为特征。
2.心脏疾病:极度的心脏肥大和肌肉无力发生于出生时看似正常的婴儿,高度提示GSD-Ⅱ。但需注意与冠状动脉起源异常、急性间质性心肌炎,特别是心内膜弹力纤维增生症相鉴别。GSD-Ⅲ型和Ⅳ型病人,虽然心肌也有一些异常结构的糖原贮积,但不导致明显心肌功能障碍。肝脏及心脏活组织切片显示溶酶体酸性α-葡萄糖苷酶缺乏是确诊GSD-Ⅱ的依据。也可通过测定肌肉组织或白细胞酶对GSD-Ⅱ病人做出诊断。产前诊断可经羊水细胞中酶的测定予以确定。也有报告用电子显微镜直接观察不经培养的羊水细胞而做出产前诊断者。
治疗方案
预后及预防
预后:婴儿型常在1 岁之内死亡;儿童型病情进展较慢,常因反复呼吸道感染而致命,也有患者可生存20 年以上;成人型预后较好。
预防:预测本病的方法是妊娠14~16 周作宫内穿刺和羊水细胞培养测定其酸性麦芽糖活性,若见降低,则应中止妊娠。
遗传病治疗困难,疗效不满意,预防显得更为重要。预防措施包括避免近亲结婚,推行遗传咨询、携带者基因检测及产前诊断和选择性人工流产等,防止患儿出生。
疾病预防
Ⅱ型糖原累积病是一种致死性的糖原累积病,而且进展速度非常快。GAA酶替代疗法的早期应用可以明显改善患者的预后,所以对此病的早期诊断和治疗变得尤为重要。这首先需要临床医生熟悉本病的特点,以免误诊和漏诊阿。其次,虽然各种诊断方法不断出现,但还没有一种或几种快速准确便捷的诊断方法。遗传病治疗困难,疗效不满意,预防显得更为重要。预防措施包括避免近亲结婚,推行遗传咨询、携带者基因检测及产前诊断和选择性人工流产等,防止患儿出生。随着对Ⅱ型糖原累积病研究的不断深入,对其进行快速准确的基因诊断将成为可能,这也为各种治疗方法的进一步研究创造了条件。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。