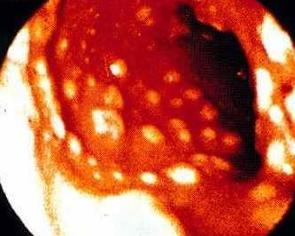
食管克罗恩病
疾病概述
克罗恩病(Crohn’s disease)是一种胃肠道的慢性、非特异性的全壁层肉芽肿性炎症,病变呈节段性分布,可累及从口腔到肛门整个消化道的一段或可同时侵犯若干段。病变部位分布中小肠、回肠末段约占90%,其他少见部位发生率大约是:口腔8%~9%,食管不足1%,胃和十二指肠0.5%~5%,肛周1%~3%。本病在1761 年首先由Morgagni 所报告,此后的一个多世纪相继有一些报告。1932 年Crohn 等发表数篇论文再次强调本病具有独特临床和病理特点。初期认为只是回肠末段的肉芽肿性炎性病变,故曾称为节段性或末段性(回)肠炎(segmental or terminal ileitis)、局限性肠炎(regional enteritis)、肉芽肿性肠炎(granulomatous enteritis)等。直到1952 年后才认识到本病可累及广泛结肠和消化道其他部位。1973 年世界卫生组织医学科学委员会建议定名为Crohn 病(克罗恩病)。食管克罗恩病(Crohn’s disease of esophagus)广义地讲,是指克罗恩病累及食管,食管病变是整个克罗恩病的一部分,大多数伴发有广泛的胃肠道克罗恩病,并有胃肠道外表现。
疾病病因
(一)发病原因
1.感染
由于其病理学表现类似结核病,过去有人认为本病可能由结核杆菌引起,现在多认为克罗恩病是由病毒感染而引起的,但未证明任何病毒和本病的发病有关。
2.遗传
临床资料显示在同一家族成员中的发病率本病较高,在不同种族间的发病率有明显差别,提示其发生可能和遗传因素有关,但尚未发现遗传规律,可能与多基因或多因子控制的遗传有一定关系。
3.免疫反应
因本病主要病理改变是肉芽肿性炎症,属于迟发型变态反应常见的组织学变化,目前有人认为克罗恩病的发病与免疫反应有关,并且在组织培养中,其循环淋巴细胞对自体或同种(包括胎儿)结肠上皮细胞有细胞毒作用;约半数病人的血清中发现抗结肠上皮细胞抗体或出现循环免疫复合物,提示存在体液免疫异常,本病常出现肠外损害,如关节炎,虹膜睫状体炎,硬化性胆管炎等,且经肾上腺皮质激素治疗后能使病情缓解,提示存在细胞免疫异常,上述特点表明克罗恩病可能是自体免疫性疾病,但在克罗恩病的发生与发展中,免疫反应的作用,地位和确切的发病机制有待于进一步研究。
(二)发病机制
1.大体标本所见
Madden等(1969)认为食管克罗恩病在大体标本上最为突出的特点是病变累及食管壁的全层,即病变过程呈透壁性,病变浸润肌层并导致受累食管黏膜层缺血性坏死,继而糜烂,脱落,形成浅表性溃疡,Gad(1989)报告的食管克罗恩病病例中,33%在显微镜下可见典型的微小肉芽肿,如无肉芽肿性改变,则其他组织学改变如黏膜水肿,糜烂,溃疡形成,淋巴管扩张以及炎症等表现,可作为食管克罗恩病的诊断依据。
2.镜下所见
食管克罗恩病最显著的组织学改变亦为非干酪性上皮样肉芽肿,这种肉芽肿由上皮样组织细胞聚集而成,可伴有Langhans多核巨细胞,其边缘有淋巴细胞环绕,中心无干酪性坏死;可见于管壁全层,但以黏膜下层最多见,其镜下特点为:病变呈透壁性改变,表现为肉芽肿或微小肉芽肿形成,多位于食管黏膜下,外膜下,肌间隙和引流区的淋巴结中,约60%的病例具有这一特点,另外还表现为局灶性淋巴细胞集聚,黏膜下层明显增厚(组织水肿,淋巴管和血管扩张及淋巴组织增生所致)。
病理生理
所有部位的克罗恩病均有相似的病理特点。炎症可累及食管壁全层,但以黏膜下层和外膜病变为多见,类似复发性小肠克罗恩病的病理过程。食管黏膜结构破坏,可见纵行线状溃疡,深溃疡或裂隙深入至增厚的黏膜下层,甚至贯通至外膜面。一旦形成穿透,便可形成窦道和瘘管。受累及的食管可造成管腔狭窄、梗阻。炎症涉及食管壁各层,伴有淋巴细胞、组织细胞浆细胞浸润。食管克罗恩病最显著的病理组织学改变为,食管非干酪样肉芽肿,呈弥漫性或结节性淋巴样聚集,黏膜下层高度增宽。
流行病学
如Weterman 报告的31 例食管克罗恩病中,有16 例合并其他部位病变。狭义的食管克罗恩病是指仅限于食管受累的克罗恩病,很罕见。食管很少是惟一的克罗恩病受累器官。我国几宗较大系列报道的克罗恩病,有关克罗恩病的病变分布部位中无食管部位。国内至今仅有少数或个案病例报告。文献中大多数有关克罗恩病的研究报告男女发病率相当,但60 岁以上的克罗恩病以女性为多(2∶1)。克罗恩病患者的同胞兄弟姊妹的患病率是一般人群的17~35 倍。食管克罗恩病确切的发病率尚不清楚。儿童食管克罗恩病发病率高于成人发病率,尤其见于兼有回肠和结肠两者病变的儿童。
症状体征
一些患者急性突发起病(flare-up),急性期食管克罗恩病因有食管炎或食管溃疡常引起吞咽疼痛,疼痛多位于胸骨后。口腔、咽部可见溃疡,会阴部亦可出现溃疡。经皮质类固醇治疗可能使食管溃疡愈合。一些患者可发展为慢性病变,这种全壁层的炎症和狭窄可导致吞咽困难和吞咽疼痛、恶心,患者常伴有食欲不振、倦怠、体重减轻。可伴有发热、关节痛、结节性红斑、贫血、口眼皮肤舍格伦综合征(干燥综合征)等胃肠道外表现。急性期血沉增快。少数食管克罗恩病患者无症状,往往经内镜或X 线检查才发现和进一步进行检查确诊。
诊断检查
诊断:在诊断思路和诊断程序上,对于有原因未明的吞咽疼痛、吞咽困难、胸骨后疼痛、恶心、呕吐、呕血症状的患者应考虑到食管炎症性病变和肿瘤的可能性。一般均应进行常规的食管X 线检查和内镜检查(包括经内镜活检病理组织学检查)。如活检病理检查未提示食管癌或其他恶性肿瘤时,除应考虑其他食管炎外,尚应考虑食管克罗恩病。对于疑似病例,若能追查到食管外克罗恩病累及的其他部位,尤其是小肠、回肠末段、口腔、肛门病变时,这对食管克罗恩病的诊断是很有意义的旁证和依据。但由于病变好发于黏膜固有层或黏膜下层,所以经内镜活检难以达到深部组织,有时对黏膜深层炎性病变不能作出诊断。手术前诊断食管克罗恩病的可能较小。
实验室检查:外周血象呈轻、中度贫血;白细胞计数一般正常,病情活动特别是存在并发症时可升高;血小板计数明显升高,且与炎症活动程度相关。病变活动时血清第Ⅷ凝血因子升高,血沉增快,C 反应蛋白及其他急性时相性反应物如α1 抗胰蛋白酶、α1 抗糜蛋白酶、α2 球蛋白、β2 微球蛋白、A 淀粉样蛋白等均可升高。新蝶呤是单核巨噬细胞受活化T 淋巴细胞分泌的γ干扰素诱导后释放的物质,当细胞免疫改变时,尿新蝶呤增多,其水平与病情严重程度呈负相关。血清溶菌酶活力在CD 及其他肉芽肿病变时均可升高。血清血管紧张素转换酶亦为肉芽肿病变的标志物,但在CD 时其活力正常或降低。近年还发现,抗酿酒酵母抗体可能是CD 的特异性标志物。
其他辅助检查:
1.放射学检查 X 线食管造影可见黏膜增厚、不规则,溃疡形成,呈卵石样外形;管腔狭窄,呈漏斗状或管状;也可见到瘘管。
2.内镜检查 内镜下见到的最早期食管黏膜变化为多发性、境界清晰的隆起性小红斑,其周围黏膜正常。随病情进展,在上述病变基础上形成口疮样溃疡,单个或多个,大小不一,直径为0.1~1.5cm,邻近黏膜外观可完全正常。这种溃疡是内镜诊断CD 的重要依据。如病情进一步发展,溃疡增大成线形,长约0.5~3.0cm、宽0.5~1.0cm、深0.1~0.5cm,边缘呈挖掘状;有些溃疡覆盖由坏死碎屑组成的膜。由于炎症侵犯黏膜下层,使其表面的黏膜层高低不平。还可见到黏膜架桥。内镜直视下在口疮样溃疡边缘活检,但因取得的标本较小,能检获肉芽肿的阳性率仍不足50%。因此,食管活检发现肉芽肿可作出CD 诊断;如未发现,不能排除CD。
鉴别诊断
当肉芽肿性食管炎独立存在时,还需与食管结核病、食管真菌病鉴别,主要通过涂片染色、细菌或真菌培养鉴定抗酸杆菌或真菌予以鉴别。食管克罗恩病与食管结节病(sarcoidosis of esophagus)鉴别较难。结节病是一种多系统器官的肉芽肿性疾病,多侵犯肺和肺门淋巴结,偶尔累及食管,亦可出现食管全壁层非干酪性肉芽肿样病变。该病亦可引起食管管腔内狭窄或纵隔肿大的结节外压食管,导致吞咽困难。结节病肉芽肿在组织切片上可见上皮样细胞的聚集,其中有多核巨噬细胞,周围有淋巴细胞,在巨噬细胞的胞质中可见到包涵体,如Schaumann 小体和星状小体。若能通过内镜活检或其他途径获取病理组织学检查,结合临床资料及有关检查综合分析判断,可能有助于诊断。
并发症状
治疗方案
治疗方法主要包括皮质类固醇、氨基水杨酸、免疫抑制药等药物的应用和营养支持治疗。
1.药物治疗
(1)皮质类固醇:为中、重度患者活动期首选药。作用机制是抑制磷脂酶A2,减少白细胞介素1(IL-1)、白三烯(LT)和血小板活化因子(PAF)等炎性介质的生成,消除炎症反应,减轻中毒症状。常用制剂为泼尼松(prednisone)或泼尼松龙prednisolone),0.25~0.75mg/(kg?d)。疗程6~8 周。布地奈德(布地缩松)是新型皮质类固醇制剂,抗炎作用强,为泼尼松龙的15 倍,用量为9mg/d。由于不良反应发生率低,故疗程可以较前二者疗程长,尤为适于兼作维持治疗用药。不像回肠或结肠克罗恩病后缓解慢、难以痊愈,食管克罗恩病对皮质类固醇治疗反应较好,食管溃疡病灶愈合能力相对较强。D’Haens 等报道的一组14 例患者,经皮质类固醇治疗后12 例平均随访5.3 年,其中痊愈8 例,病变持续者3 例,复发者3 例。
(2)免疫抑制药:包括硫唑嘌呤(azathioprine)、巯嘌呤(6-巯基嘌呤)和甲氨蝶呤(氨甲喋呤),作为特异性核糖核酸合成抑制剂,可抑制T 细胞介导的免疫反应而起抗炎作用。由于此类药物作用慢,一般用药3~6 个月方起效,故主要用于:
①经皮质类固醇等治疗无效者或长期依赖此类药物或出现严重不良反应者。
④作为手术前后用药。
(3)氨基水杨酸类制剂:包括柳氮磺吡啶(sulfasalazine)、美沙拉秦(5-氨基水杨酸)、美沙拉秦(4-氨基水杨酸)。此类药物主要用于局限于小肠的克罗恩病,而且与泼尼松联用并不优于单用泼尼松的疗法。鉴于此类药物疗效尚不确定,故很少用于治疗食管克罗恩病。近年,William 等根据循证医学,荟萃分析,评价治疗克罗恩病的主要常用药物,建议:对于轻、中度的克罗恩病患者,可选用泼尼松、泼尼松龙或布地奈德(布地缩松)中任一种,疗程8~16 周,复发者(6~12 周内)再用一疗程,以后可用硫唑嘌呤、巯嘌呤(6-巯基嘌呤)或甲氨蝶呤(氨甲喋呤)维持治疗。需长期治疗者可用布地奈德(布地缩松)(6~9mg/d),作为免疫抑制药的替代治疗,尤其是已中断免疫抑制药或对泼尼松有依赖者。
2.对症及支持治疗
(1)抗分泌剂:为减轻食管炎症症状、促进溃疡愈合,治疗食管克罗恩病常并用抗分泌剂如质子泵抑制剂或H2-受体拮抗药,以减少胃酸分泌和缓解胃食管酸反流。尤其是在应用皮质类固醇期间和合并有克罗恩病累及胃十二指肠者,并用抗分泌剂甚为有效。
(2)营养支持治疗:多数食管克罗恩病患者均有不同程度的营养不良,系因吞咽疼痛、进食困难、畏食、摄入不足以及炎症性疾病本身引起的消耗增加。营养支持治疗十分重要。应及时补充少渣的要素饮食,进食困难、有食管瘘管形成、不能保证热量需求者,应予全胃肠道外营养(total parenteral nutrition,TPN)。
治疗流程
A术前检查患者首先进行身体体征检查,符合生物修复治疗临床标准后才能进行治疗;
C培养在符合国际标准的GMP实验室进行生物修复因子分离、提纯、培养扩增;
注:在此过程中,临床医生、实验员将对提取过程进行严格监控,对修复因子质量进行评估,保证生物修复因子的安全性、有效性。
D回输生物修复因子输入的途径主要是介入、腰穿、静脉回输等方式。
注:一个疗程生物修复治疗分两次回输修复因子,第一次回输与第二次回输的时间间隔为2~3周。(患者就医当日上午采集骨髓血后,下午即可完成第一次回输)
疾病预防
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。