巨细胞病毒病
疾病概述
巨细胞病毒(cytomegalovirus,CMV)感染目前已日益受到重视;因受染细胞呈巨细胞化,胞质、胞核内可见包涵体,故又名巨细胞包涵体病(cytomegalicinclusion disease,CID)。受染后病毒可局限于涎腺,有的则导致全身性感染。显性感染者则有多样化的临床表现,严重者可致死。由于巨细胞病毒可经宫内感染造成死胎、流产、早产,也可导致先天畸形。人群普遍易感,年龄越小,易感性越高,临床表现也越重。
病因
一、病因
CMV归属于人疱疹病毒科β亚科,具有明显的宿主种属特异性。CMV对外界抵抗力差,65℃加热30min、紫外线照射5min、乙醚等均可使之灭活,亦不耐酸。
二、发病机制
 人一旦发生CMV感染,常终身带毒,可侵入肺、肾、肝、肠道、视网膜等脏器及唾液腺、乳腺其他腺体和多核白细胞和淋巴细胞,可长期或间隙地自唾液、乳、汗、血液、尿液、精液、子宫分泌物多处排出病毒。免疫正常时可无症状,但病毒仍潜伏持续存在,主要潜伏部位是血管内皮细胞及血管平滑肌细胞,此外也潜伏于淋巴细胞、单核细胞、多形核白细胞、上皮细胞及成纤维细胞。
人一旦发生CMV感染,常终身带毒,可侵入肺、肾、肝、肠道、视网膜等脏器及唾液腺、乳腺其他腺体和多核白细胞和淋巴细胞,可长期或间隙地自唾液、乳、汗、血液、尿液、精液、子宫分泌物多处排出病毒。免疫正常时可无症状,但病毒仍潜伏持续存在,主要潜伏部位是血管内皮细胞及血管平滑肌细胞,此外也潜伏于淋巴细胞、单核细胞、多形核白细胞、上皮细胞及成纤维细胞。
CMV(巨细胞病毒)感染可引起机体的免疫功能降低,特别是细胞免疫功能下降。
CMV感染对胸腺发育及脾细胞、单核吞噬细胞、NK细胞及CTL细胞的功能有着显著的影响。受染细胞变性,体积增大呈巨细胞化,然后崩解,导致局部坏死和炎症。
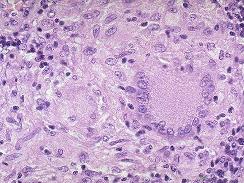
受染细胞发生巨细胞样变后具有以下特点:
(1)细胞体积:显著肿大,达10~40 μm;
(2)胞核:也变大;内可见嗜酸性包涵体,呈红色,周围绕以透亮晕环,与核膜分开,使其整个外观状似猫头鹰眼。
(3)胞质:显得相对较少;且其内也可能出现包涵体。
症状体征
1.后天感染 多呈隐性感染或症状轻微,但少数患者临床表现较为严重。围生期感染的新生儿患者(其中部分可能系在宫内受染)可呈迁延性肺炎;儿童及成人患者可发生巨细胞病毒性肝炎(症状体征类似于一般病毒性肝炎)。有的患者可表现为畏寒、发热、咽痛、头痛、身痛、血中出现变异淋巴细胞,可高达10%~20%,其临床表现颇似于EB 病毒感染所致的传染性单核细胞增多症,但嗜异性凝集试验呈阴性,可资鉴别。据统计,在传染性单核细胞增多症患者中,大约8%系因CMV 感染所致。对机体处于免疫抑制状态的患者,CMV 感染可导致严重的临床表现。由于器官移植术受者常须接受免疫抑制处理,故CMV 感染是器官移植术后严重并发症的主要病因之一,如肝炎、溃疡性胃肠道炎、肺炎等;有的可导致术后死亡,或被迫摘除已移植的器官。此类患者的CMV 感染主要来源于供者(供体器官及移植手术所需的大量输血中均可能潜伏有CMV 感染),但亦可能系因患者原有CMV 隐伏感染的激活,不过后者的病情可能较前者为轻。人巨细胞病毒病也常见于HIV(人类免疫缺陷病毒)感染者。HIV 感染发病成为艾滋病患者后,则易形成全身播散性CMV 感染,系艾滋病患者的一个重要死因。
2.宫内感染 系孕妇体内的CMV 通过胎盘使胎儿在宫内受染,是人巨细胞病毒病感染的重要途径之一。受染胎儿90%为隐性感染,仅10%表现为临床感染,但有时后果较为严重,尤其当感染发生在妊娠头4 个月内时,更易造成胎儿损害。例如,部分受染胎儿呈现发育迟缓,出生时体重不足,或呈各种形式的先天畸形,如小头畸形、肢体畸形、先天性心脏病、斜眼、失明等,或在出生后短期内出现黄疸、肝脾肿大、肺炎、心肌炎、出血倾向、嗜睡、昏迷、抽搐等多系统器官损害,可于数星期内死亡。CMV 宫内感染也可造成死胎、流产、早产。在一组3810 的新生儿流行病学调查中,脐血标本的抗-CMV-IgM 的阳性检出率为1.5%;而在该组40 例死产、死胎的脐血标本中,抗-CMV-IgM 的阳性检出率则高达32.5%。
诊断检查
诊断:凡新生儿、婴幼儿患间质性肺炎,或患肝炎伴单核细胞增多,出现变异淋巴细胞,尤其伴有先天畸形的新生儿,应考虑本病。成人接受输血、器官移植,或免疫抑制治疗后出现单核细胞增多,出现变异淋巴细胞,发热、皮疹、肝脾肿大者,亦应考虑本病。本病患者嗜异性凝集试验呈阴性,可与EB 病毒所致的传染性单核细胞增多症相鉴别。鉴别诊断时尚应注意与病毒性肝炎以及其他病因所致的肝大、黄疸等相区别。对于先天性畸形,或死胎、流产、早产等所谓“TORCH综合征”的患者,则应与导致此类疾患的其他病因即弓形虫病、风疹病毒感染、单纯疱疹病毒感染,及其他可能的病原体感染(如梅毒螺旋体等)一一鉴别。外周血抗-CMV IGM 阳性表明新近存在CMV 感染,对于婴幼儿患者可诊断本病。由于孕妇外周血IgM 型抗体不能通过胎盘屏障,所以若新生儿脐血抗-CMV IgM检测阳性则可诊断CMV 宫内感染(采集脐血标本时应注意避免母血污染)。婴幼儿外周血仅单一抗-CMV IgG 检测阳性者,应连续随访6~12 个月,观察其滴度是否有显著意义的升高。由于成人人群中CMV 抗体检出率很高,故检测CMV 抗体用于成人患者诊断本病的意义有限。用PCR 技术检测患者标本中的巨细胞病毒基因有助于确诊本病;可早在出生后头3 周,就能从新生儿的尿液或唾液标本中检测出CMV 的存在,为CMV 的宫内感染提供依据。
近年有报道,对于肾移植手术的阳性供者和受者,利用高灵敏度的试剂盒定量检测其血清CMV 抗原滴度,可有助于决定是否进行抗病毒治疗。
实验室检查:较重患者可有白细胞数增高,血中出现变异淋巴细胞;婴幼儿患者常伴贫血、血小板数减少;累及肝脏导致CMV 肝炎的患者出现肝功能异常。利用PCR 技术进行CMV 基因检测,可提供病毒在患者体内存在的直接证据;其灵敏度很高,可在数小时内做出检测报告,已成为临床诊断CMV 感染或带毒状态的重要手段;但须在经过技术认证合格的实验医学实验室内进行,并在操作过程中应注意避免污染,严格控制反应条件,以排除PCR 技术可能导致的假阳性反应。采集患者尿液、唾液、血液或活检组织标本接种人二倍体成纤维细胞进行体外培养、分离病毒可确诊本病;不过,CMV 生长缓慢,接种后4~6 周始能观察到培养细胞病变,不能用需要复杂的设备条件,故临床上仍难以普遍推广应用。细胞涂片病理学检查或活组织病理学检查均可望查见特征性的巨细胞样变细胞及胞核内嗜酸性包涵体,有助于本病的诊断,但其检出率并不高,且不能仅以此作为确诊的依据。若采用细胞免疫组织化学技术进行CMV 抗原的检测,可以提高阳性检出率,而且能据此确诊。
其他辅助检查:免疫电镜:做病毒鉴定。
治疗方案
本病迄今尚无满意的抗病毒治疗药物。阿昔洛韦对本病无效。更昔洛韦和膦甲酸钠是两种治疗CMV 感染的抗病毒药物,已用于艾滋病患者、器官移植术后合并CMV 感染患者的治疗,或器官移植术后的预防性用药,不过临床使用后的效果尚未臻理想。
更昔洛韦是阿昔洛韦的衍生物,实验室观察可抑制巨细胞病毒DNA 的合成。临床试用于巨细胞病毒病患者的剂量为:缓慢静脉滴注更昔洛韦2.5mg/kg 体重,1 次/8h,或5mg/kg 体重,1 次/12h,共2~3 周。经初步观察,此药有一定近期疗效,但停药后病毒又可重新复制活跃,故需用药维持数月,甚至数年;由于此药有一定毒性,例如使白细胞、血小板数减少等,故而往往难以坚持长期使用。对阿昔洛韦过敏者亦禁用此药。此外,临床上已发现一些CMV 毒株对更昔洛韦表现出不同程度的耐药性;而且,此药对巨细胞病毒性肺炎无效。膦甲酸钠对巨细胞病毒DNA 聚合酶和HIV 病毒反转录酶均有抑制作用,故临床试用于治疗巨细胞病毒和HIV 病毒合并感染的患者。
预防预后
预后:一般成人或儿童患者发生CMV临床感染后大多预后良好。对机体处于免疫抑制状态的患者,例如器官移植术受者、艾滋病患者、接受化疗或放疗的晚期癌症患者,CMV感染可导致严重的临床表现,或加速其死亡。CMV宫内感染可导致流产或死产。
预防:对CMV 抗体阳性的孕妇须加强围生期医学保健,必要时,抽取羊水进行CMV 抗体的检测,阳性者(尤其抗-CMV IgM 阳性)则提示已发生CMV 宫内感染。据调查表明,此类妇女再度妊娠后发生胎儿CMV 宫内感染的概率则减少,故可与患者夫妇讨论本次妊娠是否考虑人工流产。尤其对本次宫内感染发生的时间可能系在妊娠头4 个月内,且本次妊娠又属该例妇女首次受孕者,具有CMV 宫内感染的较高风险。人工流产可能有利于优生优育。但若患者夫妇因某种缘故不易受孕,本次妊娠属珍贵儿,则不能贸然做出决断,可辅以B 超检查胎儿协助决策。加强对器官移植(包括骨髓移植)供者的巨细胞病毒病筛选措施,包括对用于器官移植手术过程中所需血源的巨细胞病毒病筛选,均有助于预防巨细胞病毒病或潜伏性感染的发作,提高器官移植术的成功率。预防巨细胞病毒病的疫苗业已研制出来,尚在观察试用中。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。

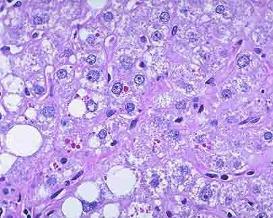 巨细胞病毒(cytomegalovirus,CMV)感染
巨细胞病毒(cytomegalovirus,CMV)感染