氯化钠
化合物简介
基本信息
英文名称:sodium chloride
英文别名:sodium hydrochloride; Sodium chloride
CAS号:7647-14-5
分子式:NaCl
分子量:58.44280
精确质量:57.95860
安全信息
海关编码:2501002000
WGK Germany:1
危险类别码:R36; R22
安全说明:S24/25-S26
RTECS号:VZ4725000
危险品标志:Xi
物理性质
外观与性状:无色晶体或白色粉末
密度:2.165g/cm³(25℃)
折光率:1.378
水溶解性:360 g/L (25 ºC)
稳定性:在正常运输和装卸条件下稳定。
蒸汽压:1 mm Hg ( 865 °C)
熔点:801℃
沸点:1465℃
氯化钠是白色无臭结晶粉末。熔点801℃,沸点1465℃,微溶于乙醇、丙醇、丁烷,在和丁烷互溶后变为等离子体,易溶于水,水中溶解度为35.9g(室温)。NaCl分散在酒精中可以形成胶体,其水中溶解度因氯化氢存在而减少,几乎不溶于浓盐酸。无臭味咸,易潮解。易溶于水,溶于甘油,几乎不溶于乙醚。
化学性质
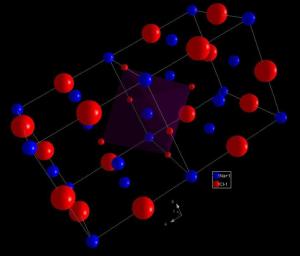
氯化钠的晶体形成立体对称。其晶体结构中,较大的氯离子排成立方最密堆积,较小的钠离子则填充氯离子之间的八面体的空隙。每个离子周围都被六个其他的离子包围着。这种结构也存在于其他很多化合物中,称为氯化钠型结构或石盐结构。
1.电解熔融态氯化钠制取金属钠
2.电解食盐水
3.与硝酸银反应
离子方程式:(其实质为Cl
(concentrated代表浓,excess代表过量)
5.NaCl的检验
一:向氯化钠溶液中滴入硝酸酸化过的硝酸银溶液,有白色沉淀(氯化银沉淀)产生,证明有Cl-。
二:用铂丝蘸取少量溶液,置于酒精灯上灼烧,火焰呈黄色,可证含有Na+。
三:为了消除干扰,可取原试液加饱和氢氧化钡至呈明显碱性,这时大部分阳离子和PO43−、AsO43−等阴离子都将被沉淀。引入试液中的Ba2+应继以碳酸铵除之,最后用灼烧法除去铵盐。残渣用水加热浸取后,取溶液以HAc酸化,按1:8的滴数加乙酸铀酰锌试剂,并用玻璃棒摩擦管壁,如有柠檬黄色结晶形沉淀生成,示有Na+存在。
制备方法
工业方法
 由海水(平均含2.4%氯化钠)引入盐田,经日晒干燥,浓缩结晶,制得粗品。亦可将海水,经蒸汽加温,砂滤器过滤,用离子交换膜电渗析法进行浓缩,得到盐水(含氯化钠160~180g/L)经蒸发析出盐卤石膏,离心分离,制得的氯化钠95%以上(水分2%)再经干燥可制得食盐。还可用岩盐、盐湖盐水为原料,经日晒干燥,制得原盐。用地下盐水和井盐为原料时,通过三效或四效蒸发浓缩,析出结晶,离心分离制得。
由海水(平均含2.4%氯化钠)引入盐田,经日晒干燥,浓缩结晶,制得粗品。亦可将海水,经蒸汽加温,砂滤器过滤,用离子交换膜电渗析法进行浓缩,得到盐水(含氯化钠160~180g/L)经蒸发析出盐卤石膏,离心分离,制得的氯化钠95%以上(水分2%)再经干燥可制得食盐。还可用岩盐、盐湖盐水为原料,经日晒干燥,制得原盐。用地下盐水和井盐为原料时,通过三效或四效蒸发浓缩,析出结晶,离心分离制得。
实验室方法
将粗盐溶于水中,去除不溶性杂质,再加精制剂如氢氧化钠和碳酸钠等,使SO42-、Ca2+、Mg2+等可溶性杂质变成沉淀,过滤除去,最后用纯盐酸将pH调节至7,浓缩溶液即得纯氯化钠结晶。
储存方法
操作注意事项:密闭操作,加强通风。操作人员必须经过专门培训,严格遵守操作规程。建议操作人员佩戴自吸过滤式防尘口罩,戴化学安全防护眼镜,穿防毒物渗透工作服,戴橡胶手套。避免产生粉尘。避免与氧化剂接触。搬运时要轻装轻卸,防止包装及容器损坏。配备泄漏应急处理设备。倒空的容器可能残留有害物。
应用领域
工业
1、电解氯化钠水溶液时,会产生氢气和氯气,氯气在化工中有很广泛的应用,可以用于合成聚氯乙烯、杀虫剂、盐酸等。
2、当斯法制取金属钠:通过电解熔融氯化钠和氯化钙的混合物制取金属钠。氯化钙用作助熔剂,可将氯化钠的熔点降低至700℃以下。钙的还原性不及钠,不会引进杂质。
3、氯化钠是许多生物学反应所必需的,如分子生物学试验中多种溶液配方都含有氯化钠,细菌培养基中大多含有氯化钠。同时也是氨碱法制纯碱时的原料。
4、无机和有机工业用作制造烧碱、氯酸盐、次氯酸盐、漂白粉的原料、冷冻系统的致冷剂,有机合成的原料和盐析药剂。钢铁工业用作热处理剂。高温热源中与氯化钾、氯化钡等配成盐浴,可作为加热介质,使温度维持在820~960℃间。此外、还用于玻璃、染料、冶金等工业。
6、侯氏制碱法制纯碱:第二步:把第一步制得的碳酸氢铵溶液与氯化钠溶液混合,在10℃下得到碳酸氢钠和氯化铵。
食品工业
在烹调菜肴中加入食盐可以除掉原料的一些异味,增加美味,这就是食盐的提鲜作用。“淡无味,咸无味”是说用盐量要适当,才能发挥其特有的功能。
医用
 氯化钠对于地球上的生命非常重要。大部分生物组织中含有多种盐类。血液中的钠离子浓度直接关系到体液的安全水平的调节。由信号转换导致的神经冲动的传导也是由钠离子调节的。
氯化钠对于地球上的生命非常重要。大部分生物组织中含有多种盐类。血液中的钠离子浓度直接关系到体液的安全水平的调节。由信号转换导致的神经冲动的传导也是由钠离子调节的。
含氯化钠0.9%的水称为生理盐水,因为它与血浆有相同的渗透压。生理盐水是主要的体液替代物,广泛用于治疗及预防脱水,也用于静脉注射治疗及预防血量减少性休克。
人类与其他灵长类不同,人类通过出汗分泌大量的氯化钠。
氯化钠是人所不可缺少的。成人体内所含钠离子的总量约为60g,其中80%存在于细胞外液,即在血浆和细胞间液中。氯离子也主要存在于细胞外液。钠离子和氯离子的生理功能主要有:
(1)维持细胞外液的渗透压;
(3)氯离子在体内参与胃酸的生成,此外,氯化钠在维持神经和肌肉的正常兴奋性上也有作用。
农业
其水溶液可用于选种。按物种需要配置NaCl溶液,其密度比水大。种子放入NaCl溶液,漂浮的不饱满,沉下的饱满。
其他
根据新加坡科技研究属发布的新发现揭示,氯化钠可以显著提高硬盘的容量。具体来讲,现有的传统硬盘采用的是随机分配的磁片存储技术,每平方英寸只能达到0.5TB的数据密度。而新的技术得益于氯化钠的帮助,配合新的高分辨率光刻因子技术,数据数据密度将更加有序,可以达到3.3TB每平方英寸而无需复杂的设备升级。使1TB的硬盘采用这种技术,无需增加盘片就能达到6TB的容量。
安全措施
危险性
危险性类别:本品不属于危险品范畴。
健康危害:食用过多容易血压升高。建议中老年人群尽量少食。
燃爆危害:不易燃易爆。
急救措施
皮肤接触:皮肤接触后用清水清洗干净即可。
食入:如食用过量,应当多喝水(如:喝糖水、喝盐开水)或者使用其他措施(例如:注射生理盐水)来维持体内的盐分,否则,后果很严重(会呈人体脱水症状)。
消防措施
危险特性:本品属于无毒性化工产品,不易燃,对消防无特殊要求。
有害燃烧产物:无有害燃烧产物。
泄漏应急处理
氯化钠无危险性,直接处理即可。
操作处置与储存
储存注意事项:应储存于阴凉、常温避光、通风干燥处,可以垛放,防止雨淋、不得与酸碱混存、垛底要铺放木板,用以防潮,垛放高度不超过两米。
接触控制
眼睛防护:如果氯化钠晶体进入眼睛,要用大量水冲洗。
相关新闻
烹饪误区
2012年8月12日,央视科教频道《健康之路》节目中,专家金锋称,炒菜时早放盐,可以让氯化钠的氯挥发出去,就剩下钠了。这一观点被网友认为是违反化学常识。中国农业大学食品学院营养与食品安全系副教授范志红表示,氯化钠是稳定的化合物,在烹调温度下不会分解,不可能发生氯挥发的情况。8月16日,金锋表示,在节目中的言论未经过验证,有失严谨和妥当。
新化合物
2013年12月,科研人员如今利用先进的理论理解力和极端条件,将精制食盐转化成了奇特化学物。盐由钠和氯构成。实验结果表明,在压强为20-142吉帕斯卡的条件下,氯化钠可以转化为三氯化钠、一氯化三钠、一氯化二钠、二氯化三钠和七氯化钠这样的奇特化学物而且保持住了稳定的化学特性。
药典标准
来源含量
性状
本品在水中易溶,在乙醇中几乎不溶。
鉴别
本品显钠盐与氯化物的鉴别反应(2010年版药典二部附录Ⅲ)。
检查
酸碱度
取本品5.0g,加水50ml溶解后,加溴麝香草酚蓝指示液2滴,如显黄色,加氢氧化钠滴定液(0.02mol/L)0.10ml,应变为蓝色;如显蓝色或绿色,加盐酸滴定液(0.02mol/L)0.20ml,应变为黄色。
溶液的澄清度与颜色
取本品5.0g,加水25ml溶解后,溶液应澄清无色。
碘化物
取本品的细粉5.0g,置瓷蒸发皿内,滴加新配制的淀粉混合液(取可溶性淀粉0.25g,加水2ml,搅匀,再加沸水至25ml,随加随搅拌,放冷,加0.025mol/L硫酸溶液2ml、亚硝酸钠试液3滴与水25ml,混匀)适量使晶粉湿润,置日光下(或日光灯下)观察,5分钟内晶粒不得显蓝色痕迹。
溴化物
取本品2.0g,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取5ml,置10ml比色管中,加苯酚红混合液[取硫酸铵25mg,加水235ml,加2mol/L氢氧化钠溶液105ml,加2mol/L醋酸溶液135ml,摇匀,加苯酚红溶液(取苯酚红33mg,加2mol/L氢氧化钠溶液1.5ml,加水溶解并稀释至100ml,摇匀,即得)25ml,摇匀,必要时,调节pH至4.7]2.0ml和0.01%的氯胺T溶液(临用新制)1.0ml,立即混匀,准确放置2分钟,加0.1mol/L的硫代硫酸钠溶液0.15ml,用水稀释至刻度,摇匀,作为供试品溶液;另取标准溴化钾溶液(精密称取在105℃干燥至恒重的溴化钾30mg,加水使溶解成100ml,摇匀,精密量取1ml,置100ml量瓶中,用水稀释至刻度,摇匀,即得。每1ml溶液相当于2μg的Br)5.0ml,置10ml比色管中,同法制备,作为对照溶液。取对照溶液和供试品溶液,照紫外-可见分光光度法(2010年版药典二部附录ⅣA),以水为空白,在590nm处测定吸光度,供试品溶液的吸光度不得大于对照溶液的吸光度(0.01%)。
硫酸盐
取本品5.0g,依法检查(2010年版药典二部附录ⅧB),与标准硫酸钾溶液1.0ml制成的对照液比较,不得更浓(0.002%)。
亚硝酸盐
取本品1.0g,加水溶解并稀释至10ml,照紫外-可见分光光度法(2010年版药典二部附录Ⅳ A)测定,在354nm波长处测定吸光度,不得过0.01。
磷酸盐
取本品0.40g,加水溶解并稀释至100ml,加钼酸铵硫酸溶液[取钼酸铵2.5g,加水20ml使溶解,加硫酸溶液(56→100)50ml,用水稀释至100ml,摇匀]4ml,加新配制的氯化亚锡盐酸溶液[取酸性氯化亚锡试液1ml,加盐酸溶液(18→100)10ml,摇匀]0.1ml,摇匀,放置10分钟,如显色,与标准磷酸盐溶液(精密称取在105℃干燥2小时的磷酸二氢钾0.716g,置1000ml量瓶中,加水溶解并稀释至刻度,摇匀,精密量取1ml,置100ml量瓶中,用水稀释至刻度,摇匀,即得。每1ml相当于5μg的PO4)2.0ml用同一方法制成的对照液比较,不得更深(0.0025%)。
亚铁氰化物
取本品2.0g,加水6ml,超声处理使溶解,加混合液[取硫酸铁铵溶液(取硫酸铁铵1g,加0.05mol/L硫酸溶液100ml使溶解)5ml与1%硫酸亚铁溶液95ml,混匀]0.5ml,摇匀,10分钟内不得显蓝色。
铝盐
(供制备血液透析液、血液过滤液或腹膜透析液用)取本品20.0g,加水100ml溶解,再加入醋酸-醋酸铵缓冲液(pH 6.0)10ml,作为供试品溶液;另取标准铝溶液[精密量取铝单元素标准溶液适量,用2%硝酸溶液定量稀释制成每1ml含铝(Al)2μg的溶液]2.0ml,加水98ml和醋酸-醋酸铵缓冲液(pH 6.0)10ml,作为对照品溶液;量取醋酸-醋酸铵缓冲液(pH 6.0)10ml,加水100ml,作为空白溶液。分别将上述三种溶液移至分液漏斗中,各加入0.5%的8-羟基喹啉三氯甲烷溶液提取三次(20、20、10ml),合并提取液置50ml量瓶中,加三氯甲烷至刻度,摇匀。照荧光分析法(2010年版药典二部附录Ⅳ E),在激发波长392nm、发射波长518nm处测定,供试品溶液的荧光强度应不大于对照溶液的荧光强度(千万分之二)。
钡盐
取本品4.0g,加水20ml溶解后,滤过,滤液分为两等份,一份中加稀硫酸2ml,另一份中加水2ml,静置15分钟,两液应同样澄清。
钙盐
取本品2.0g,加水10ml使溶解,加氨试液1ml,摇匀,加草酸铵试液1ml,5分钟内不得发生浑浊。
镁盐
取本品1.0g,加水20ml使溶解,加氢氧化钠试液2.5ml与0.05%太坦黄溶液0.5ml,摇匀;生成的颜色与标准镁溶液(精密称取在800℃炽灼至恒重的氧化镁16.58mg,加盐酸2.5ml与水适量使溶解成1000ml,摇匀)1.0ml用同一方法制成的对照液比较,不得更深(0.001%)。
钾盐
取本品5.0g,加水20ml溶解后,加稀醋酸2滴,加四苯硼钠溶液(取四苯硼钠1.5g,置乳钵中,加水10ml研磨后,再加水40ml,研匀,用质密的滤纸滤过,即得)2ml,加水使成50ml,如显浑浊,与标准硫酸钾溶液12.3ml用同一方法制成的对照液比较,不得更浓(0.02%)。
干燥失重
取本品,在105℃干燥至恒重,减失重量不得过0.5%(2010年版药典二部附录Ⅷ L)。
铁盐
取本品5.0g,依法检查(2010年版药典二部附录Ⅷ G),与标准铁溶液1.5ml制成的对照液比较,不得更深(0.0003%)。
重金属
取本品5.0g,加水20ml溶解后,加醋酸盐缓冲液(pH 3.5)2ml与水适量使成25ml,依法检查(2010年版药典二部附录Ⅷ H第一法),含重金属不得过百万分之二。
砷盐
取本品5.0g,加水23ml溶解后,加盐酸5ml,依法检查(2010年版药典二部附录Ⅷ J第一法),应符合规定(0.00004%)。
含量测定
取本品约0.12g,精密称定,加水50ml溶解后,加2%糊精溶液5ml、2.5%硼砂溶液2ml与荧光黄指示液5~8滴,用硝酸银滴定液(0.1mol/L)滴定。每1ml硝酸银滴定液(0.1mol/L)相当于5.844mg的NaCl。
类别
电解质补充药。
贮藏
密封保存。
制剂
氯化钠注射液
 功能主治:本品各种原因所致的失水,包括低渗性、等渗性和高渗性失水;高渗性非酮症糖尿病昏迷,应用等渗或低渗氯化钠可纠正失水和高渗状态;低氯性代谢性碱中毒;外用生理盐水冲洗眼部、洗涤伤口等;还用于产科的水囊引产。
功能主治:本品各种原因所致的失水,包括低渗性、等渗性和高渗性失水;高渗性非酮症糖尿病昏迷,应用等渗或低渗氯化钠可纠正失水和高渗状态;低氯性代谢性碱中毒;外用生理盐水冲洗眼部、洗涤伤口等;还用于产科的水囊引产。
用法用量:
1. 高渗性失水 高渗性失水时患者脑细胞和脑脊液渗透浓度升高,若治疗使血浆和细胞外液钠浓度和渗透浓度过快下降,可致脑水肿。故一般认为,在治疗开始的48小时内,血浆钠浓度每小时下降不超过0.5mmol/L。
若患者存在休克,应先予氯化钠注射液,并酌情补充胶体,待休克纠正,血钠>155mmol/L,血浆渗透浓度>350mOsm/L,可予0.6%低渗氯化钠注射液。待血浆渗透浓度<330mOsm/L,改用0.9%氯化钠注射液。补液总量根据下列公式计算,作为参考:所需补液量(L)= [血钠浓度(mmol/L)-142] ×0.6×体重(Kg)。
一般第一日补给半量,余量在以后2~3日内补给,并根据心肺肾功能酌情调节。
2. 等渗性失水 原则给予等渗溶液,如0.9%氯化钠注射液或复方氯化钠注射液,但上述溶液氯浓度明显高于血浆,单独大量使用可致高氯血症,故可将0.9%氯化钠注射液和1.25%碳酸氢钠或1.86%(1/6M)乳酸钠以7∶3的比例配制后补给。后者氯浓度为107mmol/L,并可纠正代谢性酸中毒。补给量可按体重或红细胞压积计算,作为参考。
(1) 按体重计算:补液量(L)=[体重下降(kg)×142]/154;
(2) 按红细胞压积计算:补液量(L)=[实际红细胞压积-正常红细胞压积×体重(kg)×0.2]/正常红细胞压积。正常红细胞压积男性为48%,女性为42%。
3. 低渗性失水 严重低渗性失水时,脑细胞内溶质减少以维持细胞容积。若治疗使血浆和细胞外液钠浓度和渗透浓度迅速回升,可致脑细胞损伤。一般认为,当血钠低于120mmol/L时,治疗使血钠上升速度在每小时0.5mmol/L,补超过每小时1.5mmol/L。
当血钠低于120mmol/L时或出现中枢神经系统症状时,可给予3%~5%氯化钠注射液缓解滴注。一般要求在6小时内将血钠浓度提高至120mmol/L以上。补钠量(mmol/L)=[142-实际血钠浓度(mmol/L)]×体重(kg)×0.2。待血钠回升至120~125mmol/L以上,可改用等渗溶液或等渗溶液中酌情加入高渗葡萄糖注射液或10%氯化钠注射液。
4. 低氯性碱中毒给予0.9%氯化钠注射液或复方氯化钠注射液(林格氏液)500~1000ml,以后根据碱中毒情况决定用量。
不良反应:
1. 输液过多、过快,可致水钠潴留,引起水肿、血压升高、心率加快、胸闷、呼吸困难,甚至急性左心衰竭。
禁忌:尚不明确。
注意事项:1. 下列情况慎用:
(1) 水肿性疾病,如肾病综合征、肝硬化、腹水、充血性心力衰竭、急性左心衰竭、脑水肿及特发性水肿等。
(2) 急性肾功能衰竭少尿期,慢性肾功能衰竭尿量减少而对利尿药反应不佳者。
2. 根据临床需要,检查血清中钠、钾、氯离子浓度;血液中酸碱浓度平衡指标、肾功能及血压和心肺功能。
性状:本品为无色的澄明液体;味微咸。
儿童用药:补液量和速度应严格控制。
老年用药:补液量和速度应严格控制。
药物相互作用:作为药物溶剂或稀释剂时,应注意药物之间的配伍禁忌。
药理作用:氯化钠是一种电解质补充药物。钠和氯是机体重要的电解质,主要存在于细胞外液,对维持正常的血液和细胞外液的容量和渗透压起着非常重要的作用。正常血清钠浓度为135~145mmol/L,占血浆阳离子的92%,总渗透压的90%,故血浆钠量对渗透压起着决定性作用。正常血清氯浓度为98~106mmol/L,人体中钠、氯离子主要通过下丘脑、垂体后叶和肾脏进行调节,维持体液容量和渗透压的稳定。
药代动力学:氯化钠静脉注射后直接进入血液循环,在体内广泛分布,单主要存在与细胞外液,钠离子,氯离子均可被肾小球滤过,并部分被肾小管重吸收,有肾脏随尿排泄,仅少部分从汗排出。
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。

