辅酶
定义
由于辅酶在 酶催化反应中其化学组分发生了变化,因此可以认为辅酶是一种特殊的 底物或者称为“第二底物”。这种所谓的第二底物可以被许多酶所利用。例如,目前已知有约七百种酶可以利用辅酶NADH进行催化。
在细胞内,反应后的辅酶可以被再生,以维持其胞内浓度在一个稳定的水平上。例如,NADPH可以通过 磷酸戊糖途径和甲硫氨酸腺苷基转移酶作用下的S-腺苷基蛋氨酸来再生。由于辅酶的再生对于维持酶反应体 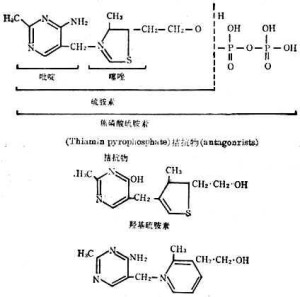 系的稳定是必要的,因此,辅酶 再生系统获得了大量的实验室以及工业应用。
系的稳定是必要的,因此,辅酶 再生系统获得了大量的实验室以及工业应用。
常见的辅酶
硫胺素
 即维生素B1。它在生物体内的辅酶形式是 硫胺素焦磷酸 (TPP)(图1[硫胺素焦磷酸(TPP)的 结构式])。
即维生素B1。它在生物体内的辅酶形式是 硫胺素焦磷酸 (TPP)(图1[硫胺素焦磷酸(TPP)的 结构式])。
硫胺素焦磷酸过去也称为 辅羧酶。它在动物 糖代谢中起着重要作用,例如 丙酮酸在 脱羧作用时需要它。在TPP缺少的情况下,代谢中间物丙酮酸不能顺利 脱羧会积聚于血液和组织中而出现神经炎症状。TPP 还是其他酶例如 -酮酸氧化酶、 转酮醇酶的辅酶。TPP催化的酶反应还需要有 镁离子的存在。
烟酰胺
是一系列酶类的辅酶的前体。
很早就知道 烟酰胺可以防止 糙皮病。1904年已知 酒精发酵时不能缺少一种叫 辅酶Ⅰ的物质,1933年这种辅酶Ⅰ被分离出来。1934年德国生化学家O.瓦尔堡又分离出一个与辅酶Ⅰ相近似的物质,称为 辅酶Ⅱ,并证实了烟酰胺是这两种辅酶的组成部分,现在已经弄清楚辅酶Ⅰ的化学组成是 烟酰胺腺嘌呤二核苷酸 (NAD),辅酶Ⅱ的化学组成为 烟酰胺腺嘌呤二核苷酸磷酸(NADP)。
以NAD(和NADP(为辅酶的酶,称为 吡啶核苷酸(或烟酰胺核苷酸)连接的 脱氢酶。这些酶催化细胞内的 氧化还原反应。一般说来,与NAD(相连的脱氢酶类通常与呼吸过程有关,而与NADP(相连的则与 生物合成反应有关。
辅酶I
(NAD)
化学名为烟酰胺腺嘌呤二核甘酸或二磷酸烟苷,在哺乳动物体内存在氧化型(NAD+)和还原型(NADH)两种状态,是人体氧化还原反应中重要的辅酶。同时,它是NAD+依赖型ADP核糖基转移酶的唯一底物,这类酶在体内主要有三种:1.ADP核糖基转移酶或聚核糖基聚合酶(PARP);2.环ADP核糖合成酶(cADPR synthases) ;3.III蛋白型赖氨酸去乙酰化酶Sirtuins。这类酶将辅酶I(NAD+)作为底物分解成ADP核糖和烟酰胺(Nam),在不同细胞中发挥不同生理功能 。
核黄素
即维生素B2。参与组成两种辅酶,是细胞内的氧化还原系统的主要成分,它们是 黄素单核苷酸(FMN)和 黄素腺嘌呤二核苷酸(FAD)。
FMN和FAD是一系列黄素连接的 氧化还原酶或称为 黄素蛋白类的辅酶,从它们与 酶蛋白结合紧密的程度来说,也可认为是辅基。这些酶中有的除了FMN或FAD外,还需要一些金属辅助因子,如铁或钼离子等。因此它们被称为 金属黄素蛋白。这些酶催化一系列可逆或不可逆的细胞中的氧化还原反应。
吡哆醛及其衍生物
吡哆醛、 吡哆胺和 吡哆醇总称为 维生素B6(图3[维生素的结构式]的结构式" class=image>)。维生素B6参与形成两种辅酶,即吡哆醛磷酸和吡哆胺磷酸。
生物素
作为一些酶的辅基而起 辅因子作用。它以 共价键的形式通过 酰胺键和 脱辅基酶蛋白的一个专一赖氨酰残基的ε- 氨基相连。ε-N-生物素酰-L-赖氨酸称为生物胞素(biocytin) (图4[生物素作为辅基的形式])。
需要生物素的酶类能催化二氧化碳的参入 (羧化作用)或转移,因而生物素和二氧化碳的固定密切相关。在羧化作用时还需要腺苷三磷酸(ATP)和镁离子的存在,此外生物素在 蛋白质生物合成中以及转氨基作用中也起着重要作用。
泛酸
最初作为酵母的生长因子被分离出来。由于在生物中广泛存在,因而被称为 泛酸。泛酸的辅酶形式是 辅酶A(CoA或CoASH),是酶促 乙酰化作用的辅助因子(图5[辅酶A的结构式]),在生物学上的重要性是作为酰基的载体或供体,在代谢上尤其是 脂肪酸的代谢上甚为重要。
叶酸
叶酸的辅酶形式是 四氢叶酸(图6[四氢叶酸的结构式]),它作为酶促转移一碳 基团(如甲酰基等)的中间载体而在 嘌呤类、 丝氨酸、甘氨酸和甲基基团的生物合成中起作用。此外,叶酸在 核蛋白的生物合成上也是不可缺少的。
维生素B12
在20年代已经发现给病人吃动物的肝能治疗恶性贫血,说明肝中有一种因子对恶性贫血有效。现在 维生素B12已经被 分离提纯并且结构也已弄清。维生素B12的结构中有一个咕啉(corrin)环系统,并且含有钴离子及  氰基(CN),故又称 氰钴胺素。纯净的 维生素B12溶液呈红色,这也是一般钴化合物的特征。作为辅酶时,维生素B12中的CN被5'-脱氧腺苷基团所代替,称为 辅酶B12。这是一个不稳定的化合物,当有 氰化物存在或暴露于光照下即转变为维生素B12。如以5'-脱氧腺苷基代替式中的黑体-CN基,就是辅酶B12的结构式。
氰基(CN),故又称 氰钴胺素。纯净的 维生素B12溶液呈红色,这也是一般钴化合物的特征。作为辅酶时,维生素B12中的CN被5'-脱氧腺苷基团所代替,称为 辅酶B12。这是一个不稳定的化合物,当有 氰化物存在或暴露于光照下即转变为维生素B12。如以5'-脱氧腺苷基代替式中的黑体-CN基,就是辅酶B12的结构式。
意义
维生素B族辅酶
在几种重要的代谢反应中起作用。在二羧酸的异构作用中,例如在 谷氨酸转化为甲基天冬氨酸的酶促反应中,在 乙二醇和 甘油转化为醛类,生物合成甲基基团以及 核苷的合成中需要辅酶B12
其他重要辅酶 除了 B族维生素成员组成了大部分重要的辅酶以外,在生物化学上重要的还有 辅酶Q、 谷胱苷肽、 尿苷二磷酸葡糖(UDPG)、 维生素K族等。
其他重要的辅酶
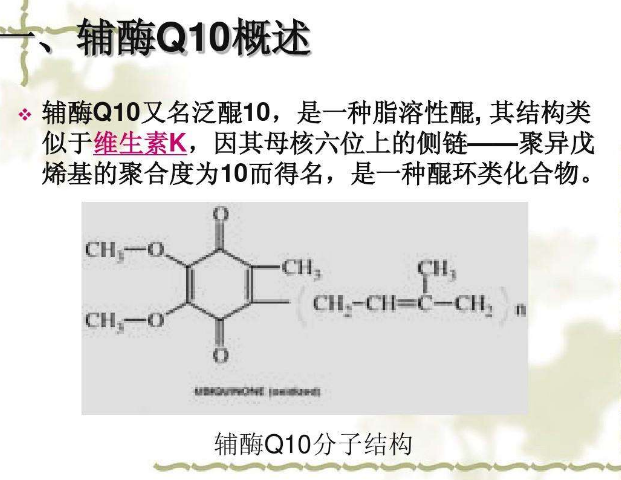
1、辅酶Q(CoQ) 辅酶 Q是生物体内广为分布的一类醌类物质,又称为 泛醌。存在于 线粒体内膜中,是 生物氧化 呼吸链中的一个不可缺少的氢递体,具有重要的生理意义。辅酶 Q侧链的 异戊二烯单位的长度对于不同的 生物种可以是不同的。
2、 谷胱甘肽(Glutathion) 谷胱甘肽是一个小分子量的胞内三肽,即γ-L-谷 氨酰-L-半胱氨酰 甘氨酸在大多数生物细胞中,谷胱甘肽的主要作用是保护一些蛋白质的 巯基以维持它们在还原状态。谷胱甘肽还在生物体内产生的 过氧化氢还原上起一定作用,但这些都不是辅酶的作用。谷胱甘肽也作为一些酶的辅酶而起作用,例如它是 乙二醛酶(Glyoxalase)及顺丁烯二酸单酰 乙酰乙酸 异构酶(Maleoylacetoacetate isomerase) 的辅酶。谷胱甘肽也是体内甲醛氧化成 甲酸反应的辅酶。
3、 尿苷二磷酸葡糖 (UDPG) 是 核苷二磷酸糖类的一种,作为辅酶主要是在糖类合成中起作用。其他可作为辅酶的核苷二磷酸糖类有尿苷二磷酸半乳糖(UDPGal)、尿苷二磷酸甘露糖(UDPMan)等,他们在糖类 合成代谢中是非常重要的。例如 UDPG 作为半乳糖-4- 表异构酶(Galactose-4-epimerase)的辅酶,在D-半乳糖的代谢中起作用:
D-半乳糖-1-磷酸+UDPG[355-04]
UDPGal+D-葡萄糖-1-磷酸
4、维生素K族 维生素K族中的某些成员可能在生物体内起某些辅酶作用。如作为辅酶在 谷氨酸残基的羧化作用中的功能已获得一些线索。
5、 甲基萘醌类(Menaquinone,即 维生素K2类)很可能是某些细菌中使 二氢乳清酸转变为乳清酸反应的酶的辅酶。
易混淆的分类
根据酶 催化反应最适条件的要求,原则上在酶测定体系中应加入一定量的辅助因子。辅助因子(cofactors)是指酶的活性所需要的一种非蛋白质成分,包括辅酶、辅基和金属离子激活剂。与酶紧密结合的辅因子称为辅基;不含辅基的酶蛋白称为 脱辅基酶蛋白(apoenzyme),没有 催化活性,必须加入足量辅基,和它结合成为 全酶(holoenzyme),才有催化活性。脱辅基酶蛋白与辅基孵育一段时间后,酶活性才会恢复,因此,往往需要样品与试剂中的辅基先预孵育的过程。辅基的用量往往较少。
与酶蛋白结合很松弛,用透析和其它方法很易将它们与酶分开的称为辅酶(Coenzyme)。辅酶尽管不同于酶的底物,但在作用方式上和底物类似,在 酶反应过程中与酶结合、分离及反复循环。辅酶用量的确定可将它们按底物处理。例如乳酸脱氢酶中辅酶按双底物动力学方程计算。
激活剂(activator)的化学本质是金属离子,可以是 酶的活性中心,也可以通过其他机制激活酶的活性。作为激活剂的金属离子,其影响 酶促反应的动力学更加复杂。最常见的是二价金属离子如Mg2+、Zn2+、Mn2+、Ca2+、Fe2+等。 重金属离子大多是酶的变性剂。金属离子之间往往存在相互拮抗或相互抑制。在酶测定体系中经常加入EDTA目的是螯合一部分非必要的离子。合适的金属离子浓度是必要的,过量的离子往往抑制酶 反应速度。由于激活剂的动力学往往与酶的动力学不同,这就可以解释不同的 样品与反应液的比例,造成酶活性测定结果的不呈比例。 N-乙酰半胱氨酸对 肌酸激酶的 激活作用与此类似。激活剂的用量一般通过反复实验来确定。
辅酶Q-10有助于为 心肌提供充足氧气,预防突发性心脏病,尤其在心肌缺氧过程中 辅酶Q10发挥关键作用。
(2)促进能量转化,提升精力:
辅酶Q-10帮助把食物转化为细胞生存必需的能量(如ATP),使细胞保持最佳状态,使人感觉精力更充 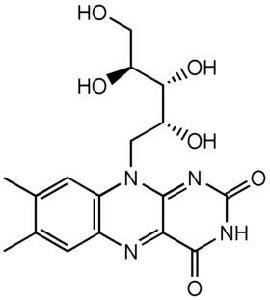 沛;
沛;
(3)提高免疫力,延缓衰老:
辅酶Q-10是细胞自身产生的 天然抗氧化剂,可阻止 自由基的形成,有助于维护免疫系统的正常运作及延缓衰老;
近年来的研究表明,辅酶Q-10在预防 冠心病,缓解牙周炎,治疗十二指肠溃疡及 胃溃疡及缓解心绞痛方面有显著效果。同时还有抗肿瘤作用,临床对于晚期转移性癌症有一定疗效。
主要的作用
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。