老年人败血症
病因
发病原因
败血症的病因绝大多数为细菌,偶可为支原体等。病原菌中以需氧菌为主,厌氧菌和真菌也占有一定比例。近年来,随着广谱抗菌药物、免疫抑制药物的广泛应用及创伤性诊疗技术的开展,使老年败血症的病原菌有了较大变迁。
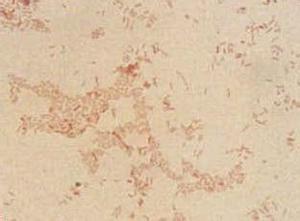 1、以革兰阴性杆菌多见 老年败血症以医院内感染多见。医院内败血症占老年败血症总数的60%左右,比中青年败血症高3倍左右。老年败血症条件致病菌所致增加。致病菌以革兰阴性杆菌为主,约占60%以上,厌氧菌有所增加,约占15.1%。较常见的致病菌是肺炎杆菌、铜绿假单胞菌、大肠埃希杆菌、产气杆菌、葡萄球菌、白色念珠菌等。
1、以革兰阴性杆菌多见 老年败血症以医院内感染多见。医院内败血症占老年败血症总数的60%左右,比中青年败血症高3倍左右。老年败血症条件致病菌所致增加。致病菌以革兰阴性杆菌为主,约占60%以上,厌氧菌有所增加,约占15.1%。较常见的致病菌是肺炎杆菌、铜绿假单胞菌、大肠埃希杆菌、产气杆菌、葡萄球菌、白色念珠菌等。
2、复数菌感染常见 老年人免疫功能低下,老年败血症可以出现多种细菌混合感染,使病情加重,治疗困难。老年败血症复数菌感染者占17.6%,多为1~3种。
3、耐药菌多 老年败血症以院内感染多见,条件致病菌败血症常见,老年败血症致病菌中耐药菌株多,表现为高度和(或)多重耐药。
4、以呼吸道入侵者多见 老年败血症的感染途径以呼吸道感染后发生败血症较中青年为多。由褥疮入侵者亦不少。其他入侵途径有泌尿道、胆道和腹腔感染以及血管内留置导管等。
发病机制
发病学特点:病原菌从不同途径侵入血循环后是否引起败血症取决于人体的防御免疫功能和细菌的毒力与数量。
①机体防御免疫功能降低是败血症的最重要的诱因。增龄所致机体防御免疫减退,营养状况差,对感染的应激能力差,使老年人容易感染,并诱发败血症。
②老年人多患有较多慢性病,常有长时间住院,使感染机会增加;某些疾病过程,也使感染发生率高,如慢性支气管炎易并发肺部感染,久病卧床易发生褥疮并感染,前列腺肥大使泌尿道感染易发生,并可诱发败血症;某些药物的应用,如肾上腺皮质激素、抗代谢药、广谱抗生素、放射治疗,细胞毒类药物的应用等都可诱发败血症;手术机会增多、创伤性检查和治疗、导尿管的留置等都可诱发败血症。
并发症
症状体征
1、起病隐匿,症状不典型 由于老年人全身情况差,机体反应低下,使老年败血症起病隐匿,早期往往缺乏典型症状。体温不太高,多为中低热,热型不规则,寒战少见,甚至体温不升,提示病情严重。常仅仅表现为淡漠、嗜睡、心率加快等。
2、感染性休克多见 老年人免疫功能差,往往病情发展迅速,极易发生感染性休克,尤其是革兰阴性杆菌败血症时更易出现,常伴不同程度的意识障碍。
3、多脏器衰竭(MOF)常见 老年人机体免疫功能差,病情发展迅速而不易控制,全身各器官退化,老年败血症常出现心、肺、肝、肾、脑等重要脏器的损害,最终导致多脏器功能衰竭,如急性肾衰、昏迷、心力衰竭,呼吸衰竭,甚至肝功能衰竭,水、电解质紊乱和酸碱平衡失调、DIC等。
5、迁徙损害 老年败血症迁徙性损害较多见,是由细菌栓子播散至身体其他部位而引起。多见于化脓球菌(尤其是金葡菌)、厌氧菌等所致的败血症。常见者有肺脓肿、皮下脓肿等。易并发心内膜炎。
6、白细胞数增高不明显 老年人机体反应性较差,血白细胞增高不明显,可正常或偏低,核左移也可不明显。血小板计数下降明显。
7、多有严重的基础疾病 患者在发生败血症以前多已存在严重的基础疾病。如恶性肿瘤、血液病、糖尿病、尿毒症、慢性支气管炎和肺气肿、肝硬化和腹膜炎等,有原发病的临床表现,常使临床症状错综复杂。
老年败血症临床表现不典型,老年人机体反应差,血白细胞总数增高不明显,加上原发病感染症状往往掩盖了败血症症状,使老年败血症漏诊和误诊率高。有的病人直到血培养获得阳性结果才得以确诊,影响了早期诊断。
凡老年患者急性发热,血白细胞总数及中性粒细胞增高、正常或偏低,而无局限于某一系统的急性感染时,应考虑有败血症的可能。病史询问和详细体查对协助诊断和推测病原有一定意义。凡新近有呼吸道、泌尿道、胆道等感染病灶;或有褥疮、外伤者;或血管内留置导管等;或各种局灶感染虽经有效抗菌药物治疗,而体温仍未能控制者,均应高度怀疑有败血症的可能。如在病程中出现皮疹、迁徙性脓肿等,则败血症的临床诊断可基本确立。详细体检常可发现原发病灶或入侵途径,并可据此推知病原菌的种类。
血培养和(或)骨髓培养阳性是确诊老年败血症的依据。其中血培养最常用,为获得较高的阳性率,宜在抗菌药物应用前及寒战、高热时采血,并宜多次反复送检,每次采血量不少于5ml,如已应用抗菌药物,则可应用薄膜过滤、集菌法、血块培养法,或于培养基中加入硫酸镁、内酰胺酶、对氨苯甲酸等以破坏某些常用的抗菌药物。还应注意厌氧菌、真菌和L型细菌培养。骨髓培养的阳性率较血培养为高。以脓液、脑脊液、胸腹水、瘀点等涂片检查或培养,亦有检出病原菌的机会。分离出病原菌后应进行抗菌药物敏感试验和联合药物敏感试验以测定最低抑菌浓度(MIC),以供选用或调整抗菌药物时参考。必要时测最低杀菌浓度(MBC),血清杀菌试验也有重要参考意义。
近已开展的气相色谱(尤其是气液相色谱,GLC)法、离子色谱法(IC)等快速诊断技术亦可协同诊断老年败血症。鲎溶解物试验(LLT)可检测血清等标本中革兰阴性杆菌的内毒素,对诊断革兰阴性菌败血症有一定帮助。
检查鉴别
检查
(一)血象 血细胞总数增多,一般在(10—30)×109/L,中性粒细胞百分比增高,可出现明显核左移及细胞内中毒性颗粒,嗜酸粒细胞减少或消失。机体反应性较差者及少数革兰阴性杆菌败血症患者的白细胞总数可正常或偏低,但中性粒细胞数仍增多。
(二)病原学检查 以血培养最为重要,应在抗菌药物应用前及寒战、高热时进行、并宜多次反复送验、每次采血量新生儿和婴儿为5ml,年长儿和成人为10ml。有条件者宜同时作厌氧菌和真菌培养。已采用抗菌药物的病例宜于培养基中加入硫酸镁、β—内酰胺酶、对氨苯甲酸等以某些抗菌药物,或用血块培养法以提高阳性率。骨髓培养的阳性率较血培养者为高。以脓液、脑脊液、胸腹水液、淤点挤野等涂片检查和培养,亦有检出病原菌的机会。分离得病原菌后敏实验,以测定最低抑菌浓度(MIC),供选用抗菌药物参考。必要时测量最低杀菌浓度(MBC),血清杀菌实验也有重要参考意义。一般培养基上无细菌生长,疑有L—型细菌败血病时,应作高渗盐水培养。真菌生长缓慢,培养阳性率亦较低。乳胶凝集实验测定抗原或相应抗体(用于隐球菌病),以及病理组织检查等均有助于诊断。厌氧菌分离培养至少也需1周,不能及时为临床治疗提供细菌学依据。近年已开展气相色谱法、离子色谱法等快速诊断技术。色谱法也能在1小时内对林装标本做出有无厌氧菌的诊断,便于指导用药。免疫荧光法快速、敏感,且能特异地鉴定厌氧菌;其他尚有免疫酶表组化快速鉴定产气荚膜梭菌等,对早期诊断有良好效果。
鉴别
①疟疾:间日疟为规则的间日发作,表现突起寒战、高热继以大汗以及明显的间歇缓解期,恶性疟的发热、寒战多不规则,但白细胞总数与中性粒细胞均不高,全身中毒症状较轻,确诊靠在血片或骨髓涂片查见疟原虫;
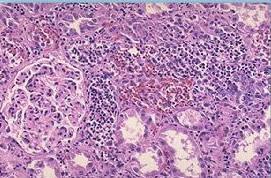 ②急性肾盂肾炎:可有高热与寒战,但常有腰痛与肾区叩痛,尿中可查见白细胞与脓细胞。尿培养有病原菌生长,血培养为阴性;
②急性肾盂肾炎:可有高热与寒战,但常有腰痛与肾区叩痛,尿中可查见白细胞与脓细胞。尿培养有病原菌生长,血培养为阴性;
③化脓性胆管炎:可有高热、寒战,但有胆绞痛史、黄疸、血清胆红素增高,胆管区有明显压痛与叩痛,血培养阴性;
④肺炎链球菌肺炎:急起高热,可有寒战,但有咳嗽、胸痛、铁锈色痰,肺部可有实变体征。X线胸片显示肺大片炎变。痰培养可有肺炎链球菌生长。血培养阴性。后三种疾病,如血培养有病原菌生长,则表明已经并发了败血症。
2、高热伴白细胞显著增高者 应与下列疾病鉴别:
①脑膜炎球菌脑膜炎:急性高热,头剧痛、呕吐、颈强直、凯尔尼格征阳性。皮肤可有瘀点与瘀斑。脑脊液呈化脓性,涂片染色镜检可见革兰阴性双球菌,血培养可能也有该菌生长,常流行于冬春季。
②流行性乙型脑炎:急起高热,意识障碍,轻度脑膜激惹征,脑脊液为非脓性,轻度白细胞增高,流行季节为夏秋。
③钩端螺旋体病:急起高热,腹股沟淋巴结肿大,压痛,腓肠肌疼痛与压痛,有一定地区性与季节性和疫水接触史。青霉素早期治疗的疗效好。
④流行性出血热:有地区性、季节性,先有发热,多不太高,数天后退热,但继以病情反而加重,出现低血压休克期,继以少尿期,甚至无尿与肾衰竭。如病情好转还可出现多尿期。早期呈酒醉貌,皮肤黏膜出血点,结膜水肿,蛋白尿。白细胞与中性粒细胞显著增高,可达(10~30)109/L以上,甚至呈类白血病反应。血培养阴性。
⑤成人斯提尔病(adult Stills disease):其临床表现的发热与白细胞增高,极似败血症。发热可持续数月之久,全身中毒症状较轻。可反复出现少数短暂性皮疹。血培养反复阴性。抗生素治疗无效。吲哚美辛类药物有一定退热效果。肾上腺皮质激素有效。
3、高热与白细胞减低者 应与下列疾病鉴别:
①伤寒与副伤寒:起病较缓,发热多呈梯形上升,1周后呈持续高热,可有玫瑰疹,听力减低。白细胞显著减低。丙型副伤寒可有迁徙性炎症。肥达反应阳性,血培养或骨髓培养可有伤寒或副伤寒沙门菌生长。
②急性粟粒型结核:起病较缓,持续高热。可无明显咳嗽,血培养阴性。起病2周后X线胸片可显示粟粒型肺结核影像。
③恶性组织细胞增多症:持续发热,多呈弛张热或不规则热,经久不退,常出现贫血,消瘦。白细胞减少。血培养多次阴性,抗生素治疗无效。血涂片、骨髓涂片与淋巴结活检可查到恶性组织细胞而确诊。
治疗方案
(一)抗菌药物的应用 败血症一经诊断,在未获得病原学结果之前即应根据情况给予抗菌药物经验治疗,以后再根据病原菌种类和药敏试验结果调整给药方案。败血症的抗菌治疗可采用两种有效抗菌药物的联合,为了保证适当的血浆和组织的药物浓度,宜静脉给药,剂量要大,应选用杀菌剂。疗程宜较长,一般3周以上,或在体温下降至正常,临床症状消失后继续用药7—10d。
(1)病原菌不能确定时须选用兼顾革兰阴性杆菌和革兰阳性球菌抗菌药物的联合,一般选用抗假单胞菌青霉素(如哌拉西林替卡西林)或第3代头孢菌联合氨基糖苷类抗生素。如果是免疫功能低下者的院内感染,应多豪华金葡菌或表葡菌及假单位胞菌,可给予去甲万古霉素联合头孢他啶。
(2)葡萄球败血症:目前葡萄球菌对抗生素的抗药现象严重,除对情绪素高度乃要外(95%以上),对头孢噻吩、头孢唑林的乃要也有增加的趋势,乃要率约30%—40%,约半数菌株对苯唑西林耐药,不同地区尚未出现了比例不等的呈多重乃要得MRSA败血症。但葡萄球菌通常对万古霉素敏感,鉴于上述情况目前对葡萄球菌败血症的应首选苯唑西林或氨唑西林,也可选用头孢噻吩或头孢唑林联合应用利福平,待获得药敏结果后则可根据药敏结果调整。MRSA及MRSE败血症则可选用万古霉素(或去甲万古霉素)磷霉素或利福平的联合应用。替代万古霉素选用药物有替靠拉宁、夫西地酸等。
(3)链球菌败血症:A、B组溶血性链球菌通常对青霉素敏感B组链球菌的敏感性略差,因此,治疗A组链球菌败血症时可单用青霉素或第一代头孢菌素、红需素与林可霉素等,而后者治疗宜加用氨基糖苷类抗生素。耐青霉素肺炎链球菌其治疗同溶血性链球菌败血症。肠球菌常对多种抗生素耐药,治疗时需联合用药,首选青霉素或氨苄西林与氨基糖苷类的联合也可选择万古霉素(或去甲万古霉素)联合氨基糖苷类。其他对肠球菌感染有效的药物尚有亚胺培南或亚胺培南和西拉司丁的复方制剂泰能。
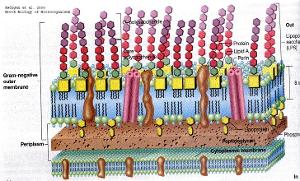 (4)革兰阴性败血症:大肠埃希菌、肺炎克雷伯杆菌等肠杆菌科细菌对氯霉素、氨苄西林等普遍耐药,对哌拉西林的敏感率高于庆大霉素。临床上可选哌拉西林、第二或第三代头孢菌素与庆大霉素或阿米卡星联合应用。铜绿假单胞等假单胞菌及不动杆菌属多数为院内感染,对哌拉西林及羧苄西林耐药者日渐增多,可根据药敏选用头孢他啶或孢哌酮,联合应用庆大霉素或阿米卡星。
(4)革兰阴性败血症:大肠埃希菌、肺炎克雷伯杆菌等肠杆菌科细菌对氯霉素、氨苄西林等普遍耐药,对哌拉西林的敏感率高于庆大霉素。临床上可选哌拉西林、第二或第三代头孢菌素与庆大霉素或阿米卡星联合应用。铜绿假单胞等假单胞菌及不动杆菌属多数为院内感染,对哌拉西林及羧苄西林耐药者日渐增多,可根据药敏选用头孢他啶或孢哌酮,联合应用庆大霉素或阿米卡星。
(5)厌氧菌败血症:首先要清除病灶或行脓肿引流以改变厌氧环境。抗菌药物选用甲硝唑、氯霉素、克林霉素、头孢西丁或亚胺培南或泰能。由于多五需氧菌或兼性厌氧菌的混合感染,因此,需同时对需氧细菌进行有效的抗菌治疗。
(6)真菌性败血症:可选用两性霉素B、氟康唑、伊曲康唑、5—氟胞嘧啶等,仍以良性霉素B抗菌作用最强,但因其毒性大,常限制其使用,此时可选用氟康唑。两性霉素B与氟康唑联合应用的疗效较好。
(7)其他:单核细胞增多性李斯特菌对青霉素高度敏感,常选用青霉素或氨苄西林。JK组棒状杆菌对万古霉素高度敏感,是最佳选择、其次是红霉素、庆大霉素等。鼠伤寒沙门菌易耐药,宜根据药敏结果选择用药一般对第二代第三代头孢菌素、氟喹诺酮类药物高度敏感。
(二)治疗局部感染病灶及原发病 化脓性病灶无论为原发性或迁徙性,均应尽早给予切开引流。化脓性心包炎、脓胸、惯技言及肝脓肿等可穿刺引流。胆道或泌尿道感染合并有梗阻者应给予手术治疗。如果病人的免疫抑制状态是由于药物或疾病所致,则须停用或减量免疫抑制药或有效治疗这些基础疾病(如白血病等)。考虑败血症由静脉留置导管而致,则应及早去除或更换,将除去导管剪一段(约1厘米)进行培养以明显病原菌。如败血症由人工关节等留置假体所至抗生素疗程须6周,且常须除去此装置。
(三)其他治疗 包括适量营养、补充维生素以及维持水与电解质平衡,并按需输血、血浆和蛋白质。近20年来还寻找新的治疗方法,如抗生素抗体的应用、抗TNF—α单克隆抗体的应用、输注粒细胞和GSF等但这些新治疗方法的疗效仍需作进一步评价。静脉注射人血清免疫球蛋白可体液免疫对抗细菌感染。
疾病预防
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。

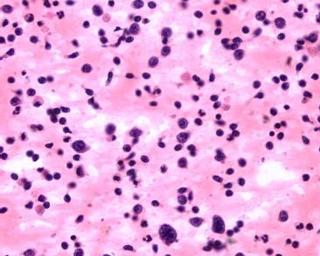
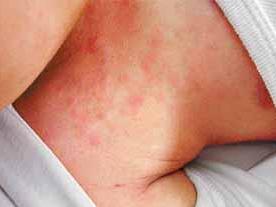 4、可有皮疹 老年
4、可有皮疹 老年