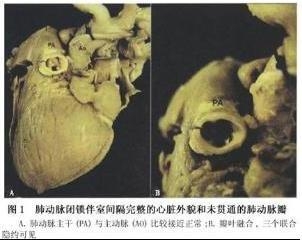
肺动脉闭锁
病因
这种先天性畸形多数单独涉及肺动脉瓣闭锁,应该与肺动脉闭锁合并圆锥动脉干畸形区别。与伴有主动脉右位和转位的复杂畸形(比如肺动脉闭锁合并室间隔缺损,伴或不伴大动脉转位)不同,圆锥动脉干的不均等分隔为该类畸形肺动脉通道发育不良的根本原因,而半月瓣与开放的右室漏斗部之间的正常连接提示肺动脉闭锁是一种原发的独立的病理改变。因为胚胎时期动脉干隆起最初是彼此分隔的结构,而三个瓣叶融合成无孔的膜状结构,说明这是发育过程后期的继发变化。尽管右室流出道闭锁,许多患儿右室的三部分仍然存在,右心室腔轻到中度发育不良。这一点支持如下理论:右心室的病理改变继发于三尖瓣反流的严重程度,三尖瓣反流影响右室充盈的情况。明显的三尖瓣反流使右心室容量增加,导致有一定大小的右心室腔。三尖瓣功能尚可伴有右室流出道梗阻时,将导致不同程度的隔壁束肥厚,甚至右室小梁部和漏斗部闭合。文献中所描述的心肌内窦隙就是肥厚的隔壁束之间的狭窄而迂回的空隙,血管造影可清晰显示这些空隙与右室小梁部典型的部位相一致。三尖瓣与肺动脉瓣环发育不良很可能是继发现象,是心室腔明显发育不良的结果。在心管形成过程中,在心管的背侧形成一些称为心系膜囊的囊性结构,最终这种结构位于两层心包反折处,其中一些心系膜囊排列成纵向隧道。隧道沿着心管的背侧缝开口于心管腔。这些系膜囊形成单层血管壁,最终发育成冠状动脉系统,以柱形开口与动脉干连接。因此冠状动脉系统与右心室窦隙之间的连接即为胚胎时期心系膜囊与右室小梁之间间隙的连接,这种胚胎时的连接可以解释在有些患者中存在冠状动脉与右心室的交通。
病理
伴有室间隔缺损又称假性总动脉干,为法洛四联症中最严重类型,由于肺动脉瓣闭锁或缺如,右心室和肺动脉之间没有通道,肺动脉干本身亦可能闭锁或发育不良。左、右两侧心室的血液全部注入主动脉肺循环的血液来自动脉导管或支气管动脉。室间隔完整多伴有右心室发育不良,右室壁很厚,三尖瓣口很小;由于右心室为一盲腔,收缩时血液返回右心房;自腔静脉回到右心房的血液只能通过未闭卵圆孔或房间隔缺损而进入左心房、左心室和主动脉。肺循环的血液来自动脉导管或支气管动脉侧支循环。
发病率
室间隔完整的肺动脉闭锁(Pulmonary Atresia with Intact Ventricular Septum,PAIVS)是一种少见的先天性心脏病,发病率占先天性心脏病的1%~1.5%,无性别差异。
临床表现
 90%以上患儿于出生时或出生后很短时间内即出现紫绀,并呈进行性加重。紫绀的程度主要取决于通过动脉导管和其他体-肺动脉交通到肺的血流量。若动脉导管小,紫绀重,存活者均有杵状指(趾)。生长发育障碍,常有活动后心悸气短,但蹲踞少见。如果体-肺交通较大,紫绀较轻,易患呼吸道感染,常可早期出现心衰。如动脉导管趋向闭合,则紫绀呈进行性加重。重症患儿动脉氧分压可降至20mmHg,血氧饱和度仅为40%左右。右心衰竭多见于三尖瓣关闭不全的患者,有肝大、浮肿及心尖区奔马律。如顺产,一般患儿可发育较好,生后有紫绀,呼吸困难和代谢性酸中毒。
90%以上患儿于出生时或出生后很短时间内即出现紫绀,并呈进行性加重。紫绀的程度主要取决于通过动脉导管和其他体-肺动脉交通到肺的血流量。若动脉导管小,紫绀重,存活者均有杵状指(趾)。生长发育障碍,常有活动后心悸气短,但蹲踞少见。如果体-肺交通较大,紫绀较轻,易患呼吸道感染,常可早期出现心衰。如动脉导管趋向闭合,则紫绀呈进行性加重。重症患儿动脉氧分压可降至20mmHg,血氧饱和度仅为40%左右。右心衰竭多见于三尖瓣关闭不全的患者,有肝大、浮肿及心尖区奔马律。如顺产,一般患儿可发育较好,生后有紫绀,呼吸困难和代谢性酸中毒。
诊断
自然病程
室间隔完整的肺动脉闭锁自然预后很差,50%的患儿于出生后两周死亡,85%的患儿于出生后6个月死亡。死亡原因主要为缺氧和代谢性酸中毒,特别容易发生在动脉导管闭合后。少数活到儿童期的病人主要靠较大的房间隔缺损和动脉导管未闭,极个别患儿靠较大的心外侧支循环活到成年。
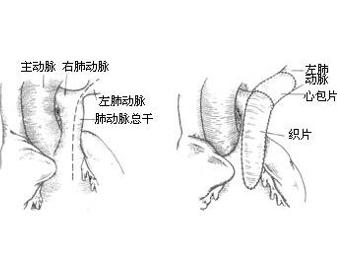
一经诊断即应手术治疗。外科大多采用分期手术治疗。生后静脉滴注前列腺素E1以延迟动脉导管闭合时间。先行体-肺动脉分流术,或同时在体外循环下行肺动脉瓣切开术;第2阶段在3~5岁时建立右室到肺动脉的血流通道,闭合房间交通和心外分流。
在新生儿期行姑息性手术的患儿,单独行肺动脉瓣切开术的存活率为27%,单独行体-肺动脉分流术的存活率为30%,同时施行上述两种手术的存活率为79%。
早期手术死亡的主要因素为分流术后吻合口大小不当。在第1次分流术后,有25%因吻合口太小需在一个月内再次手术。其次,右心室腔与冠状动脉之间的心肌冠状动脉窦交通、右心室高压、年龄及左心室功能,也是早期死亡的因素。姑息性手术后未做矫治术的3年生存率为50%,5年生存率小于30%。
根治术的早期死亡率为25%,死亡原因主要是左室功能不全。应用带瓣心外管道主要并发症是管道狭窄,需再次手术更换。长期生存的患儿心功能可恢复到Ⅰ~Ⅱ级。
检查
治疗
附件列表
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。